Bula
Combodart - 30 ComprimidosATENÇÃO: O texto abaixo deve ser utilizado apenas como uma referência secundária. É um registro histórico da bula, rótulo ou manual do produto. Este texto não pode substituir a leitura das informações que acompanha o produto, cujo fabricante podem mudar a formulação, recomendação, modo de uso e alertas legais sem que sejamos previamente comunicados. Apenas as informações contidas na própria bula, rótulo ou manual que acompanha o produto é que devem estar atualizadas de acordo com a versão comercializada porém, no caso de qualquer dúvida, consulte o serviço de atendimento ao consumidor do produto ou nossa equipe.
Bula - Combodart - 30 Comprimidos
Para que serve
Combodart é indicado para o tratamento da Hiperplasia Prostática Benigna (HPB) em homens com próstata aumentada, e prevenção da progressão dos sintomas da HPB. Ele se mostrou eficaz para:
- Aliviar os sintomas;
- Reduzir o volume da próstata;
- Melhorar o fluxo urinário e reduzir o risco de retenção urinária (bloqueio completo do fluxo de urina);
- Reduzir o risco de cirurgia relacionada a HPB.
Como o Combodart funciona?
Combodart é usado no tratamento de homens com a próstata aumentada (Hiperplasia Prostática Benigna – HPB), um crescimento não canceroso da glândula prostática causado pela ação excessiva de um hormônio chamado DHT (di-hidrotestosterona).
Combodart cápsulas é uma combinação de dois fármacos chamados dutasterida e tansulosina. A dutasterida pertence ao grupo de medicamentos chamados inibidores da 5-alfa-redutase, a tansulosina pertence ao grupo de medicamentos chamados alfa-bloqueadores.
A dutasterida reduz a quantidade de DHT que seu corpo produz e isto leva à redução do tamanho da próstata e ao alívio dos sintomas. A tansulosina age relaxando a musculatura da glândula prostática, tornando mais fácil a passagem da urina e melhorando os sintomas.
Contraindicação
Mulheres, crianças e adolescentes (menores de 18 anos) não devem manusear Combodart cápsulas, pois o ingrediente ativo pode ser absorvido através da pele. Lave imediatamente a área afetada com água e sabão caso haja qualquer contato com a pele.
Este medicamento é contraindicado para uso por mulheres e crianças.
Combodart é contraindicado em pacientes com hipersensibilidade conhecida a dutasterida, ao cloridrato de tansulosina, outros inibidores de 5-alfa-redutase ou qualquer componente da fórmula.
Como usar
Modo de usar
As cápsulas devem ser ingeridas inteiras por via oral e não podem ser ingeridas mastigadas ou abertas, pois o contato com o conteúdo da cápsula pode resultar em irritação da mucosa orofaríngea.
A tampa do frasco de Combodart possui uma trava de segurança. Para abrir o frasco, basta seguir as instruções abaixo:
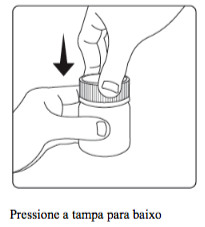
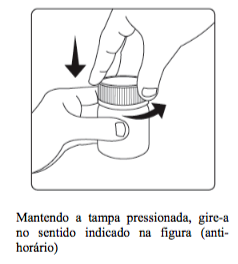
Posologia
Homens adultos (incluindo idosos)
A dose recomendada é de uma cápsula (0,5mg de dutasterida e 0,4mg de cloridrato de tansulosina) administrada por via oral, uma vez ao dia, aproximadamente 30 minutos após a mesma refeição todos os dias.
Insuficiência renal
O efeito da insuficiência renal sobre a farmacocinética de Combodart não foi estudado. No entanto, nenhum ajuste na dose é previsto para pacientes com insuficiência renal.
Insuficiência hepática
O efeito da insuficiência hepática sobre a farmacocinética de Combodart não foi estudado.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento.
Não interrompa o tratamento sem o conhecimento do seu médico.
Este medicamento não deve ser partido, aberto ou mastigado.
O que devo fazer quando eu me esqeucer de usar o Cmbodart?
Se você esquecer uma dose de Combodart, não tome cápsulas extras para compensar o esquecimento. Tome apenas a dose seguinte, no horário habitual.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
Precauções
Em estudos clínicos com a dutasterida, alguns pacientes fizeram uso de dutasterida e um medicamento alfabloqueador. Pacientes que fizeram uso desta combinação de dutasterida e um alfa-bloqueador tiveram insuficiência cardíaca com mais frequência do que pacientes que tomaram somente dutasterida ou somente o alfa-bloqueador. Não se estabeleceu relação causal entre o uso de dutasterida (sozinha ou em combinação com um alfa bloqueador (medicamento usado principalmente para tratar pressão arterial elevada)) e falência cardíaca.
Em um estudo clínico feito com mais de 8000 homens sob maior risco de câncer de próstata, 0,9% dos pacientes que recebiam dutasterida tiveram formas graves de câncer de próstata e com mais frequência do que os que não recebiam dutasterida (0,6%). Não se estabeleceu relação causal entre dutasterida e câncer de próstata de grau elevado.
Um exame de sangue que mede a quantidade de uma substância chamada de PSA (antígeno específico da próstata) no seu sangue pode ajudar seu médico a avaliar se você tem doença na próstata, incluindo câncer de próstata. Se você tem uma quantidade de PSA maior do que o normal no seu sangue isso pode significar um alto risco de você apresentar câncer de próstata.
Homens recebendo Combodart devem realizar o exame de PSA 6 meses após o início do tratamento e periodicamente depois disso. Combodart reduzirá a quantidade de PSA no seu sangue. Embora seu PSA esteja baixo, você ainda pode estar com risco de desenvolver câncer de próstata. Seu médico ainda poderá utilizar o teste de PSA para ajudar a detectar o câncer de próstata, através da comparação entre os resultados de cada teste de PSA que você fizer. É importante tomar a medicação seguindo as recomendações de seu médico. Caso não seja tomada de forma regular, isso pode interferir na capacidade de seu médico monitorar seu PSA. O exame digital retal, bem como outras avaliações para o câncer da próstata, devem ser conduzidos em pacientes com HPB, antes de iniciar o tratamento com dutasterida e periodicamente, a partir de então.
Foram relatados casos de câncer de mama em homens que tomaram dutasterida em estudos clínicos e durante o período pós-comercialização. Informe imediatamente a seu médico se você identificar alguma alteração na mama, como nódulos ou secreção no mamilo.
Se você vai se submeter a uma cirurgia de catarata, avise seu médico ou oftalmologista antes da cirurgia, que você está ou esteve fazendo uso de Combodart. Ele(a) pode pedir que você interrompa temporariamente o tratamento com Combodart.
Não tome Combodart juntamente com outro alfa-bloqueador (para próstata aumentada ou pressão alta).
Alguns medicamentos interagem com Combodart, tornando você mais propenso a ter reações adversas, eles incluem a cimetidina (para úlcera no estômago) e a varfarina (para coagulação sanguínea). Informe ao seu médico se você tem problemas hepáticos. Combodart pode não fazer bem a você.
Vazamento do conteúdo das cápsulas
A dutasterida é absorvida pela pele, portanto mulheres e crianças devem evitar o contato com as cápsulas caso estejam vazando. Se ocorrer contato com o conteúdo das cápsulas, a área afetada deve ser lavada imediatamente com água e sabão.
Reações Adversas
Combodart pode causar vertigem (tontura). Tome cuidado quando estiver deitado ou sentado e mudar para a posição sentada ou de pé, particularmente se você tiver acordado no meio da noite, até que você saiba como este medicamento lhe afeta. Se você se sentir tonto durante o tratamento, sente ou deite até que o sintoma passe.
Reações alérgicas ocorrem entre 0,1% e 1% dos pacientes que utilizam este medicamento, estes sintomas podem incluir:
Icterícia, inchaço – algumas vezes na face ou na boca (angioedema) causando dificuldade para respirar e colapso.
Reações adversas comuns (ocorrem entre 1% e 10% dos pacientes que utilizam este medicamento):
Impotência*, diminuição da libido* (baixo desejo sexual), distúrbios da ejaculação*, aumento do volume das mamas (ginecomastia) e tontura (vertigem).
* Em um número pequeno de pessoas alguns desses eventos podem continuar após a interrupção do tratamento com Combodart. O papel da dutasterida nesta persistência é desconhecido.
Reações adversas incomuns (ocorrem entre 0,1% e 1% dos pacientes que utilizam este medicamento):
Reações alérgicas, incluindo erupções na pele, coceira e urticária, batimento cardíaco acelerado (palpitação), constipação, diarreia, vômito, fraqueza (astenia), pressão baixa ao ficar de pé (hipotensão postural), nariz escorrendo, entupido ou com vontade de espirrar (rinite).
Reações adversas raras (ocorrem entre 0,01% e 0,1% dos pacientes que utilizam este medicamento):
Desmaio, alopécia (principalmente a perda de pelos do corpo), hipertricose (excesso de pelos no corpo generalizado ou localizado), síncope (desmaio), angioedema (inchaço sob a pele).
Reações adversas muito raras (ocorrem em menos de 0,01% dos pacientes que utilizam este medicamento):
Ereção persistente e dolorosa do pênis (priapismo), sintomas depressivos, reações graves na pele (tais como Síndrome de Stevens-Johnson) e dor e inchaço nos testículos. Contate imediatamente um médico se isto lhe ocorrer, você pode precisar de um tratamento para evitar complicações ainda mais graves.
Outras reações ocorreram em um número menor de pessoas, mas a sua exata frequência é desconhecida:
- Batimentos cardíacos rápidos ou anormais (arritmia ou taquicardia ou fibrilação atrial);
- Falta de ar (dispneia);
- Sangramentos nasais;
- Alterações visuais;
- Boca seca.
Atenção: Este produto é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe seu médico ou cirurgião-dentista.
População Especial
Efeitos sobre a capacidade de dirigir e operar máquinas
A tansulosina pode causar vertigem, portanto os pacientes devem ter cautela ao dirigir veículos ou operar máquinas.
Fertilidade
Não é conhecida a importância clínica do efeito da dutasterida nas características seminais vinculadas à fertilidade do paciente.
Os efeitos do cloridrato de tansulosina sobre a contagem ou a função de espermatozóides não foram avaliados.
Gravidez
A dutasterida não foi estudada em mulheres porque os dados pré-clínicos sugerem que a supressão dos níveis circulantes de di-hidrotestosterona pode inibir o desenvolvimento dos órgãos genitais externos em um feto do sexo masculino, gerado por uma mulher exposta à dutasterida.
Homens tratados com Combodart não devem doar sangue por pelo menos 6 meses após sua última dose. Essa é uma forma de prevenir que mulheres grávidas recebam a dutasterida através de transfusão de sangue.
A administração de cloridrato de tansulosina em doses superiores à terapêutica a ratas e coelhas prenhas não apresentou evidências de dano fetal.
Avise ao médico caso uma mulher grávida entre em contato com o conteúdo das cápsulas de Combodart.
Lactação
Não se sabe se a dutasterida ou a tansulosina são eliminadas no leite materno.
Este medicamento é contraindicado para uso por mulheres.
Composição
Cada cápsula contém:
| Dutasterida | 0,5mg |
| Tansulosina (equivalente a 0,4mg de cloridrato de tansulosina) | 0,37mg |
| Excipientes* | 1 cápsula |
*Excipientes: monodiglicerídeos de ácido caprílico/cáprico (MDC), butil-hidroxitolueno, cápsula gelatinosa (gelatina, glicerol, dióxido de titânio, óxido de ferro amarelo, água purificada), celulose microcristalina, copolímero de ácido metacrílico–etil acrilato, talco, citrato de trietila, cápsula de dura (carragenina, cloreto de potássio, dióxido de titânio, hipromelose, óxido de ferro vermelho, FD&C amarelo, água purificada, tinta de impressão preta).
Superdosagem
A ingestão de doses elevadas causa os mesmos eventos adversos observados em doses terapêuticas.
Não há antídoto específico para o Combodart, portanto, no caso de você usar uma grande quantidade de Combodart de uma só vez, procure socorro médico para que seja administrado tratamento sintomático e de suporte apropriado.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
Interação Medicamentosa
Não há estudos de interação medicamentosa realizados com este medicamento. As informações a seguir referem-se aos dados disponíveis dos componentes individuais.
Dutasterida
Estudos de metabolismo in vitro mostram que dutasterida é metabolizada pela isoenzima CYP3A4 do citocromo P450 humano. Portanto, as concentrações sanguíneas de dutasterida podem aumentar, na presença de inibidores de CYP3A4.
Dados de estudos de Fase II mostraram uma redução no clearance de dutasterida, quando coadministrada com os inibidores de CYP3A4 verapamil (37%) e diltiazem (44%). Em contraste, nenhuma redução no clearance foi observada com a coadministração com anlodipino ou outro antagonista dos canais de cálcio. É improvável que uma redução no clearance (e um subsequente aumento na exposição a dutasterida), na presença de inibidores de CYP3A4, seja clinicamente significativa, devido à larga margem de segurança (uma dose até 10 vezes mais alta do que a dose recomendada foi administrada a pacientes por até seis meses); portanto, nenhum ajuste da dose é necessário.
In vitro, dutasterida não é metabolizada pelas isoenzimas humanas do citocromo P450 CYP1A2, CY2A6, CYP2E1, CYP2C8, CYP2C9, CYP2C19, CYP2B6 e CYP2D6.
A dutasterida não inibe as enzimas metabolizadoras de drogas do citocromo P450 in vitro, nem induz as isoenzimas do citocromo P450 CYP1A, CYP2B e CYP3A em ratos e cães, in vivo.
Estudos in vitro demonstram que a dutasterida não desloca varfarina, acenocoumarol, femprocumona, diazepam ou fenitoína das proteínas plasmáticas, nem esses modelos de compostos deslocam a dutasterida. Os compostos que foram testados para interações medicamentosas no homem incluem tansulosina, terazosina, varfarina, digoxina e colestiramina, e nenhuma interação farmacocinética ou farmacodinâmica clinicamente significativa foi observada.
Embora estudos de interações específicas não tenham sido conduzidos com outros compostos, aproximadamente 90% dos participantes de estudos de Fase III de grande porte que receberam dutasterida estavam tomando outras medicações concomitantemente. Nenhuma interação adversa clinicamente significativa foi observada em estudos clínicos, quando a dutasterida foi coadministrada com anti-hiperlipidêmicos, inibidores da enzima conversora de angiotensina (ECA), agentes bloqueadores beta-adrenérgicos, bloqueadores dos canais de cálcio, corticosteróides, diuréticos, drogas anti-inflamatórias não esteroidais (AINEs), inibidores de fosfodiesterase Tipo V e antibióticos da classe das quinolonas.
Tansulosina
Existe o risco teórico de aumento dos efeitos hipotensivos quando o cloridrato de tansulosina é coadministrado com fármacos que podem reduzir a pressão arterial, inclusive agentes anestésicos, inibidores PDE5 e outros bloqueadores alfa-1-adrenérgicos.
Dutasterida e tansulosina não devem ser usadas em combinação com outros bloqueadores alfa-1-adrenérgicos.
A administração concomitante de cloridrato de tansulosina e cetoconazol (um forte inibidor de CYP3A4) resultou num aumento da Cmáx e da ASC do cloridrato de tansulosina por um fator de 2,2 e 2,8, respectivamente. A administração concomitante de cloridrato de tansulosina e paroxetina (potente inibidor do CYP2D6) resultou num aumento da Cmáx e da ASC do cloridrato de tansulosina por um fator de 1,3 e 1,6, respectivamente. Espera-se um aumento similar na exposição em metabolizadores fracos de CYP2D6, em comparação com metabolizadores extensos quando coadministrado com um forte inibidor de CYP3A4. Os efeitos da coadministração de ambos os inibidores de CYP3A4 e CYP2D6 com cloridrato de tansulosina não foram avaliados clinicamente, no entanto, há um potencial para o aumento significativo da exposição da tansulosina.
A administração concomitante de cloridrato de tansulosina (0,4 mg) e cimetidina (400 mg a cada seis horas durante seis dias) resultou em diminuição do clearance (26%) e aumento da ASC (44%) do cloridrato de tansulosina. Recomenda-se cautela quando este medicamento for usado em combinação com cimetidina.
Não existem ainda estudos definitivos sobre as interações medicamentosas entre cloridrato de tansulosina e varfarina. Os resultados de estudos limitados in vitro e in vivo são inconclusivos. Recomenda-se cautela quando houver administração concomitante de varfarina e cloridrato de tansulosina.
Em três estudos não foram observadas interações quando tansulosina (0,4 mg por sete dias seguidos por 0,8 mg por sete dias) foi administrada concomitantemente com atenolol, enalapril ou nifedipina por três meses; portanto, nenhum ajuste de dose é necessário quando esses fármacos são coadministrados com este medicamento.
A administração concomitante de cloridrato de tansulosina (0,4 mg/dia por dois dias, seguidos por 0,8 mg/dia por cinco a oito dias) e uma única dose intravenosa de teofilina (5 mg/kg) não resultou em alterações na farmacocinética da teofilina; portanto, nenhum ajuste de dose é necessário.
A administração concomitante de cloridrato de tansulosina (0,8 mg/dia) e uma única dose intravenosa de furosemida (20 mg) provocou uma redução de 11% a 12 % na Cmáx e ASC do cloridrato de tansulosina. Contudo, não é esperado que essas alterações tenham significado clínico e, assim, nenhum ajuste de dose é necessário.
Ação da Substância
Resultados de Eficácia
Tratamento combinado com dutasterida e tansulosina para HPB
Dutasterida 0,5 mg/dia, tansulosina 0,4 mg/dia ou a combinação de dutasterida 0,5 mg com tansulosina 0,4 mg foram avaliados em 4844 indivíduos do sexo masculino com próstatas aumentadas (? 30cc) em um estudo multicêntrico, duplo-cego, de grupos paralelos durante 4 anos.
O endpoint primário de eficácia após 2 anos de tratamento foi o nível de melhora em relação à avaliação basal na pontuação internacional de sintomas da próstata (IPSS).
A combinação de dustasterida com tansulosina forneceu uma melhora nos sintomas, superior aos tratamentos isolados com cada uma das drogas. Após 2 anos de tratamento, a combinação mostrou uma melhora média ajustada estatisticamente significativa na pontuação dos sintomas em relação à avaliação basal, de -6,2 unidades. As melhoras médias ajustadas na pontuação dos sintomas observadas com os tratamentos individuais foram de -4,9 unidades para dutasterida e -4,3 unidades para tansulosina.
A melhora média ajustada na taxa de fluxo em relação à avaliação basal foi de 2,4 ml/segundo para a combinação, 1,9 ml/segundo para dutasterida e 0,9 ml/segundo para tansulosina. A melhora média ajustada no Índice de Impacto da HPB (BII) em relação à avaliação basal foi de -2,1 unidades para a combinação, -1,7 para dutasterida e -1,5 para tansulosina.
As melhoras na taxa de fluxo e no BII foram estatisticamente significantes para a terapia combinada em relação às duas monoterapias.
A redução no volume prostático total e no volume da zona de transição, após 2 anos de tratamento, foi estatisticamente significante para a terapia combinada comparada à monoterapia com tansulosina.
O desfecho de eficácia primária aos 4 anos de tratamento foi o tempo até o primeiro evento relacionado com RUA ou cirurgia relacionada a HPB. Depois de 4 anos de tratamento, a terapia combinada reduziu de maneira estatisticamente significativa o risco de RUA ou cirurgia relacionada a HPB (65,8% de redução de risco p < 0,001 [IC 95% 54,7% a 74,1%]) em comparação com a monoterapia com tansulosina.
A incidência de RUA ou cirurgia a HPB no ano 4 foi 4,2% para a terapia combinada e 11,9% para tansulosina (p < 0,001). Em comparação com a monoterapia com dutasterida, a terapia combinada reduziu o risco de RUA ou cirurgia relacionada a HPB em 19,6%; a diferença entre os grupos de tratamento não foi significativa (p = 0,18 [IC 95% - 10,9% a 41,7%]). A incidência de RUA ou cirurgia relacionada a HPB no ano 4 foi 4,2% para a terapia combinada e 5,2% para dutasterida.
A progressão clínica foi definida como um composto de agravamento dos sintomas, (IPSS, International Prostate Symptom Score), e eventos de RUA relacionados com HPB, incontinência , ITU (infecção do trato urinário) e insuficiência renal. A terapia combinada foi associada à significância estatística da redução da taxa de progressão clínica, comparada com tansulosina (p < 0,001, 44,1% de redução de risco [IC 95%: 33,6% a 53,0%]) após 4 anos. As taxas de progressão clínica para terapia combinada, tansulosina e dutasterida foram: 12,6%, 21,5% e 17,8%, respectivamente.
A melhora média corrigida com significância estatística nos escores de sintomas (IPSS) desde o início do estudo foi mantida do ano 2 ao ano 4. As melhoras médias corrigidas nos escores de sintomas observados foram -6,3 unidades para a terapia combinada , -5,3 unidades para monoterapia com dutasterida e -3,8 unidades para a monoterapia com tansulosina.
Depois de 4 anos de tratamento a melhora média corrigida da vazão (Qmáx) desde o início do estudo foi 2,4 ml/seg para a terapia combinada, 2,0 ml/seg para monoterapia com dutasterida e 0,7 ml/seg para monoterapia com tansulosina. Em comparação com a tansulosina, a melhora média corrigida de Qmáx desde o início do estudo foi maior de modo estatisticamente significante com a terapia combinada em cada avaliação semestral do mês 6 ao mês 48 (p < 0,001). Em comparação com dutasterida, a melhora média corrigida de Qmáx desde o início do estudo não foi diferente com significância estatística do que com a terapia combinada (p = 0,050 no mês 48).
A terapia combinada foi significativamente superior (p < 0,001) à monoterapia com tansulosina e com dutasterida no tocante à melhora dos parâmetros BII de desfechos de saúde e Estado de Saúde relacionado com HPB (BHS) aos 4 anos. A melhora média corrigida de BII desde o início do estudo foi -2,2 unidade para a combinação, -1,8 para dutasterida e -1,2 para tansulosina. A melhora média corrigida de BHS desde o início do estudo foi -1,5 unidade para a combinação, -1,3 para dutasterida e -1,1 para tansulosina.
A redução do volume total da próstata e do volume da zona de transição depois de 4 anos de tratamento foi estatisticamente significante para a terapia combinada em comparação com a monoterapia somente com tansulosina.
Dutasterida
A administração de dutasterida 0,5 mg/dia ou placebo foi avaliada em 4325 indivíduos do sexo masculino, com próstatas aumentadas (mais de 30 cc) em três estudos de eficácia primária, duplo-cegos, multicêntricos, controlados com placebo, com duração de 2 anos.
Em homens com HPB, dutasterida trata e previne a progressão da doença reduzindo o risco de retenção urinária aguda (RUA) e a necessidade de intervenção cirúrgica, além de proporcionar uma melhora estatisticamente significativa dos sintomas do trato urinário inferior (STUI), da taxa de fluxo urinário máximo (Qmáx) e do volume da próstata com relação a placebo. Essas melhoras em STUI, Qmáx e volume da próstata foram observadas ao longo de 24 meses e STUI e Qmáx continuaram a melhorar por mais 2 anos nos estudos de extensão abertos. Além disso, foi mantida a redução no tamanho (volume) da próstata por mais 2 anos, em estudos de extensão abertos.
Falência cardíaca
Em comparação de quatro anos entre dutasterida (Avodart) em coadministração com tansulosina e dutasterida ou tansulosina em monoterapia em homens com HPB (do estudo CombAT), a incidência do termo composto falência cardíaca no grupo que recebeu a combinação (14/1.610 [0,9%]) foi mais alta do que nos dois grupos de monoterapia: dutasterida (4/1.623 [0,2%]) e tansulosina (10/1.611 [0,6%]). O risco relativo estimado do tempo até o primeiro evento de falência cardíaca foi de 3,57 (IC de 95%: 1,17-10,8) com o tratamento combinado em comparação com dutasterida em monoterapia e de 1,36 [IC de 95%: 0,61-3,07] em comparação com tansulosina em monoterapia.
Em um estudo comparativo de quimioprevençãode quatro anos entre placebo e dutasterida em 8.231 homens com idade entre 50 e 75 anos com biópsia prévia negativa de câncer de próstata e PSA basal entre 2,5 ng/mL e 10,0 ng/mL, (estudo REDUCE), houve maior incidência do termo composto falência cardíaca nos indivíduos que usavam dutasterida (30/4.105, 0,7%) com relação a placebo (16/4.126, 0,4%) na estimativa de risco relativo de tempo de 1,91 [IC de 95%: 1,04-3,50] até a primeira falência cardíaca. Em uma análise post hoc de uso de alfabloqueador concomitante, houve maior incidência do termo composto falência cardíaca em indivíduos que usavam dutasterida e um alfabloqueador concomitante (12/1.152, 1,0%) em comparação com os indivíduos que não usaram dutasterida e alfabloqueador simultâneo: dutasterida sem alfabloqueador (18/2.953, 0,6%), placebo e um alfabloqueador (1/1.399, <0,1%), placebo sem alfabloqueador (15/2.727, 0,6%). Não se estabeleceu relação causal entre o uso de dutasterida (isolado ou em combinação com um alfabloqueador) e falência cardíaca.
Câncer de próstata e tumores de alto grau
Em comparação de quatro anos entre placebo e dutasterida (Avodart) em 8.231 homens com idade entre 50 e 75 anos, com biópsia anterior negativa de câncer de próstata e PSA basal entre 2,5 ng/mL e 10,0 ng/mL (estudo REDUCE), 6.706 participantes tiveram dados de biópsia de próstata por agulha disponíveis para análise para determinação dos escores de Gleason. Havia 1.517 indivíduos diagnosticados com câncer de próstata no estudo. A maioria dos cânceres de próstata detectáveis por biópsia em ambos os grupos de tratamento foi diagnosticada como de baixo grau (Gleason 5-6). Não houve diferença na incidência de cânceres com escore de Gleason 7-10 (p=0,81).
Houve uma maior incidência de cânceres com escores de Gleason 8-10 no grupo de dutasterida (n=29; 0,9%), em comparação com o grupo placebo (n=19; 0,6%) (p=0,15). No 1o e 2o anos, o número de pacientes com cânceres com escores Gleason 8-10 foi similar nos grupos de dutasterida (n=17; 0,5%) e de placebo (n=18; 0,5%). No 3o e 4o anos, um número maior de casos de câncer com escores de Gleason 8-10 foi diagnosticado no grupo de dutasterida (n=12; 0,5%), em comparação com o grupo placebo (n=1; < 0,1%) (p=0,0035). Não existem dados suficientes sobre o efeito de dutasterida, além de quatro anos, em homens sob risco de câncer de próstata. A porcentagem de pacientes diagnosticados com câncer com escores de Gleason 8-10 foi uniforme entre os períodos de tempo do estudo (1o-2o anos e 3o-4o anos) no grupo de dutasterida (0,5% em cada período de tempo), enquanto que no grupo placebo a porcentagem de pacientes diagnosticados com câncer com escores Gleason 8-10 foi mais baixa durante os anos 3-4 do que nos anos 1-2 (< 0,1% vs. 0,5%, respectivamente). Em um estudo com duração de 4 anos em HPB (CombAT), no qual não havia biópsias exigidas pelo protocolo e todos os diagnósticos de câncer de próstata basearam-se em biópsias solicitadas por alguma causa, as taxas de cancêr com escores de Gleason 8-10 foram (n = 8, 0,5%) para dutasterida, (n = 11, 0,7%) para a tansulosina e (n = 5, 0,3%) para a terapia de combinação.
Os resultados de um estudo base populacional epidemiológico (n= 174.895) em cenário prático demonstraram que o uso de inibidores da 5 ?- redutase para tratar HPB/RUA não está associado com um aumento no risco de mortalidade por câncer de próstata (taxa de risco [TR] ajustada para riscos concorrentes: 0,85, 95% IC 0,72, 1,01) quando comparado com o uso de alfa bloqueadores. Resultados similares foram reportados em um estudo epidemiológico (n=13,892) com homens com câncer de próstata no Reino Unido (taxa de risco ajustada para mortalidade por câncer de próstata em usuários de inibidores da 5 ?-redutase (I5AR) versus não-usuários: 0,86; 95% IC 0,69, 1,06). Um estudo de coorte prospectivo, o “Heath Care Professional’s Follow-up Study” (n=38,058), também concluiu que o uso de I5AR não está associado com câncer de próstata fatal (TR ajustada: 0,99; 95% IC 0,58, 1,69).
Efeitos sobre o antígeno prostático específico (PSA) e detecção do câncer de próstata
No estudo REDUCE, pacientes em comparação de quatro anos entre placebo e dutasterida em 8.231 homens com idade entre 50 e 75 anos com biópsia anterior negativa de câncer de próstata e PSA basal entre 2,5 ng/mL e 10,0 ng/mL (estudo REDUCE), o tratamento com dutasterida (Avodart) causou uma redução no nível sérico médio de PSA de aproximadamente 50% depois de 6 meses de tratamento, com uma grande variabilidade (desvio padrão de 30%) entre os pacientes. A supressão de PSA observada após seis meses foi similar em homens que desenvolveram ou não câncer de próstata detectável por biópsia durante o estudo.
Incidência de câncer de mama
Em um estudo clínico com 3.374 pacientes tratados com dutasterida (Avodart) em monoterapia para HPB, houve 2 casos de câncer de mama em homens relatados, um depois de 10 semanas e um depois de 11 meses de tratamento, além de 1 caso em um paciente que recebeu placebo. Em estudos clínicos subsequentes envolvendo HPB e 8231 homens com idade entre 50 a 75 anos, com uma biópsia prévia negativa para câncer de próstata e valor basal de PSA entre 2,5 ng/mL e 10,0 ng/mL, fornececendo 17489 pacientes-ano expostos à dutasterida e 5027 pacientes-ano expostos à combinação de dutasterida e tansulosina, não houve casos de câncer de mama reportados em nenhum dos grupos de tratamento.
Em dois estudos epidemiológicos caso controlados, um conduzido nos EUA (n=339 casos de câncer de mama e n=6.780 controles) e outro no Reino Unido (n=338 casos de câncer de mama e n=3.930 controles) base de dados de hospitais, demonstraram nenhum aumento no risco de desenvolver câncer de mama em homens que usam I5AR. Os resultados do primeiro estudo não identificaram uma associação positiva para câncer de mama masculino (risco relativo para ?1 ano de uso antes do diagnóstico de câncer de mama comparado com <1 ano de uso: 0,70: 0,95% IC 0,34, 1,45). No segundo estudo, a razão de chance estimada para câncer de mama associado ao uso de I5AR comparado com o não uso foi 1,08: 95% IC 0,62, 1,87).
A relação entre o uso prolongado de dutasterida e câncer de mama masculino nãoo foi estabelecida.
Tansulosina
A tansulosina aumenta rapidamente (a partir de uma semana) o fluxo urinário máximo por meio da redução da tensão do músculo liso na próstata e na uretra, aliviando, assim, a obstrução. Também melhora o complexo de sintomas irritativos e obstrutivos nos quais a instabilidade e a tensão dos músculos lisos vesicais no trato urinário inferior têm importante papel.
Características Farmacológicas
Propriedades Farmacodinâmicas
Este medicamento é uma combinação de dois fármacos com mecanismos de ações complementares para tratar os sintomas de pacientes com HPB: dutasterida, um inibidor duplo da 5 ?-redutase (5-ARI) e cloridrato de tansulosina, um antagonista dos ?1a-adrenoreceptores.
Não é esperado que as propriedades farmacodinâmicas deste medicamento como uma combinação de dose fixa seja diferente das doses de dutasterida e tansulosina co-administradas como componentes separados.
Dutasterida
A dutasterida é um inibidor duplo da 5-alfa-redutase. Inibe as duas isoenzimas de 5-alfa-redutase, tipo 1 e tipo 2, que são responsáveis pela conversão de testosterona para 5-alfa-diidrotestosterona (DHT). DHT é o principal androgênio responsável pela hiperplasia do tecido prostático glandular.
Dutasterida reduz os níveis de DHT, reduz o volume da próstata, melhora os sintomas do trato urinário inferior e fluxo urinário e diminui o risco de retenção urinária aguda e cirurgia relacionada à hiperplasia prostática benigna.
Efeitos sobre DHT / Testosterona
O efeito máximo de doses diárias de dutasterida sobre a redução de DHT é dependente da dose, e é observado dentro de 1-2 semanas. Após 1 semana e 2 semanas de administração diária de dutasterida 0,5 mg, as concentrações séricas medianas de DHT foram reduzidas em 85% e 90%, respectivamente.
Em pacientes com HPB tratados com 0,5 mg de dutasterida diariamente, a redução mediana em DHT foi de 94% após 1 ano, e de 93% após 2 anos, e o aumento mediano dos níveis séricos de testosterona foi de 19% após 1 e 2 anos. Esta é uma consequência esperada da inibição da 5- alfa-redutase e não resultou em nenhum evento adverso conhecido.
Tansulosina
A tansulosina inibe os receptores alfa-1 adrenérgicos no estroma do músculo prostático liso e do colo da bexiga. Aproximadamente 75% dos receptores alfa-1 na próstata são do subtipo alfa-1a.
A tansulosina aumenta a taxa máxima do fluxo urinário através do relaxamento muscular da próstata e da uretra, e assim aliviando a obstrução. Ela também melhora o complexo de sintomas irritativos e obstrutivos em que a instabilidade da bexiga e tensão dos músculos lisos do trato urinário inferior desempenham um papel importante. Bloqueadores alfa-1-adrenérgicos podem reduzir a pressão arterial diminuindo a resistência periférica.
Propriedades Farmacocinéticas
Bioequivalência foi demonstrada entre este medicamento e a administração concomitante de dutasterida e tansulosina em cápsulas separadas.
O estudo de bioequivalência de dose única foi realizado em ambos estados jejum e alimentados. Uma redução de 30% em Cmáx foi observada para o componente da tansulosina no estado alimentado em comparação com o estado de jejum da tansulina-dutasterida. Os alimentos não tiveram efeito na ASC da tansulosina.
Absorção
Dutasterida
A dutasterida é administrada por via oral em solução, na forma de cápsulas gelatinosas moles. Após a administração de uma dose única de 0,5 mg, as concentrações séricas máximas de dutasterida ocorrem dentro de 1 a 3 horas.
A biodisponibilidade absoluta no homem é de aproximadamente 60%, com relação a uma infusão intravenosa de 2 horas. A biodisponibilidade de dutasterida não é afetada pelos alimentos.
Tansulosina
O cloridrato de tansulosina é absorvido do intestino e é quase completamente biodisponível.
O cloridrato de tansulosina apresenta cinética linear, depois de dose única ou múltipla, e atinge as concentrações de estado de equilíbrio no quinto dia de uma dose diária. A velocidade de absorção do cloridrato de tansulosina é reduzida por uma refeição recente. O paciente pode promover uniformidade de absorção ao tomar o cloridrato de tansulosina sempre cerca de 30 minutos após a mesma refeição a cada dia.
Distribuição
Dutasterida
Dados farmacocinéticos após doses orais únicas e repetidas mostram que a dutasterida tem um grande volume de distribuição (300 a 500 litros). A dutasterida exibe alta ligação a proteínas plasmáticas (> 99,5%).
Após a administração diária, as concentrações séricas de dutasterida atingem 65% da concentração do estado de equilíbrio após 1 mês, e aproximadamente 90% após 3 meses. Concentrações séricas no estado de equilíbrio (Css) de aproximadamente 40 nanogramas/mL são atingidas após 6 meses de administração de 0,5 mg uma vez ao dia. De maneira similar aos níveis séricos, as concentrações de dutasterida no sêmen atingiram o estado de equilíbrio após 6 meses. Após 52 semanas de tratamento, as concentrações de dutasterida no sêmen foram em média 3,4 nanogramas/mL (variação de 0,4 a 14 nanogramas/mL). O particionamento de dutasterida do soro para o sêmen foi em média de 11,5%.
Tansulosina
O volume de distribuição médio aparente do estado de equilíbrio do cloridrato de tansulosina após administração intravenosa a dez adultos saudáveis do sexo masculino foi 16 L, o que sugere distribuição para os líquidos extracelulares do corpo.
O cloridrato de tansulosina liga-se extensamente às proteínas plasmáticas humanas (94% a 99%), principalmente a glicoproteína ácida alfa-1 (AAG), com ligação linear em uma ampla faixa de concentração (20 a 600 ng/mL).
Metabolismo
Dutasterida
In vitro, a dutasterida é metabolizada pela isoenzima CYP3A4 do citocromo P450 humano para dois metabólitos secundários monoidroxilados, mas não é metabolizada por CYP1A2, CYP2A6, CYP2E1, CYP2C8, CYP2C9, CYP2C19, CYP2B6 ou CYP2D6.
No soro humano, após a administração até o estado de equilíbrio, dutasterida inalterada, 3 metabólitos principais (4’-hidroxidutasterida, 1,2- diidrodutasterida e 6-hidroxidutasterida) e 2 metabólitos secundários (6,4’-diidroxidutasterida e 15-hidroxidutasterida), conforme avaliado pela resposta espectrométrica de massa, foram detectados. Os cinco metabólitos séricos humanos de dutasterida foram detectados no soro de ratos. No entanto, a estereoquímica das adições de hidroxil nas posições 6 e 15 nos metabólitos de seres humanos e de ratos não é conhecida.
Tansulosina
Não existe bioconversão enantiomérica do cloridrato de tansulosina [isômero R(-)] para o isômero S(+), no ser humano. O cloridrato de tansulosina é metabolizado em alto grau pelas enzimas do citocromo P450 no fígado e menos de 10% da dose é excretada inalterada na urina. Contudo, o perfil farmacocinético dos metabólitos no ser humano não foi estabelecido. Os resultados in vitro indicam que CYP3A4 e CYP2D6 estão envolvidos no metabolismo de tansulosina, assim como alguma participação menor de outras isoenzimas CYP. A inibição das enzimas hepáticas metabolizadoras da droga pode levar ao aumento da exposição à tansulosina. Os metabólitos do cloridrato de tansulosina são submetidos à extensa conjugação ao glicuronídeo ou sulfato antes da excreção renal.
Eliminação
Dutasterida
A dutasterida é extensivamente metabolizada. Após administração oral de dutasterida 0,5 mg/dia até o estado de equilíbrio em seres humanos, 1,0% a 15,4% (média de 5,4%) da dose administrada são eliminados como dutasterida nas fezes. O restante é eliminado nas fezes como 4 metabólitos principais, contendo 39%, 21%, 7% e 7% cada do material relacionado à droga e 6 metabólitos secundários (menos de 5% cada um).
Apenas quantidades residuais de dutasterida inalterada (menos de 0,1% da dose) são detectadas na urina humana.
Em concentrações terapêuticas, a meia-vida terminal de dutasterida é de 3 a 5 semanas.
As concentrações séricas permanecem detectáveis (mais de 0,1 ng/mL) por até 4 a 6 meses após a descontinuação do tratamento.
Em concentrações séricas baixas (menos que 3 ng/mL), dutasterida é rapidamente eliminado por ambas as vias de eliminação, tanto concentração-dependente quanto concentração-independente. Doses únicas de 5mg ou menos apresentaram evidência de uma depuração rápida uma meia-vida curta de 3 a 9 dias.
Em concentrações séricas superiores a 3 ng/mL, dutasterida é eliminada lentamente (0,35 a 0,58 L/h), essencialmente por eliminação não saturável linear com meia-vida terminal de 3 a 5 semanas. Em concentrações terapêuticas, na sequência de doses repetidas de 0,5 mg/dia, o clearance mais lento predomina e o clearance é linear e concentração-independente.
Tansulosina
A meia-vida de tansulosina é 5 a 7 horas. Aproximadamente 10% são excretados inalterados na urina.
Idosos
Dutasterida
A farmacocinética e a farmacodinâmica de dutasterida foram avaliadas em 36 indivíduos do sexo masculino, entre as idades de 24 e 87 anos, após a administração de uma dose única de 5 mg de dutasterida. A exposição da dutasterida, representada pelos valores de ASC e Cmáx, não foi estatisticamente diferente quando comparada entre os grupos etários. A meia-vida não foi estatisticamente diferente, ao comparar o grupo de 50-69 anos de idade ao grupo de indivíduos acima de 70 anos de idade, que abrange a faixa etária da maioria dos homens com HPB. Nenhuma diferença no efeito da droga, medido pela redução de DHT, foi observada entre os grupos etários. Os resultados indicaram que não é necessário nenhum ajuste da dose de dutasterida com base na idade.
Tansulosina
A comparação em estudo cruzado da exposição geral (ASC) e da meia-vida do cloridrato de tansulosina indica que a disposição farmacocinética do cloridrato de tansulosina pode ser ligeiramente prolongada nos idosos do sexo masculino em comparação com voluntários jovens e saudáveis do sexo masculino. O clearance intrínseco é independente da ligação de cloridrato de tansulosina à AAG, mas diminui com a idade, resultando em exposição geral (ASC) 40% superior em indivíduos com idade de 55 a 75 anos, em comparação com os indivíduos com 20 a 32 anos de idade.
Insuficiência renal
Dutasterida
O efeito da insuficiência renal sobre a farmacocinética de dutasterida não foi estudado. No entanto, menos de 0,1% de uma dose de 0,5 mg de dutasterida no estado de equilíbrio é recuperado na urina humana; assim, nenhum ajuste na dose é previsto para pacientes com insuficiência renal.
Tansulosina
A farmacocinética do cloridrato de tansulosina foi comparada em 6 indivíduos com insuficiência renal leve a moderada (30 ? CLcr < 70 mL/min/1,73 m2) ou moderada a grave (10 ? CLcr < 30 mL/min/1,73 m2) e 6 indivíduos normais (CLcr > 90 mL/min/1,73 m2). Embora se tenha observado uma mudança da concentração plasmática total do cloridrato de tansulosina como resultado da ligação alterada à AAG, a concentração não ligada (ativa) do cloridrato de tansulosina, assim como o clearance intrínseco, permaneceram relativamente constantes. Portanto, os pacientes com insuficiência renal não precisam de ajuste de dose das cápsulas de cloridrato de tansulosina. Contudo, os pacientes com doença renal em estágio terminal (CLcr < 10 mL/min/1,73 m2) não foram estudados.
Insuficiência hepática
Dutasterida
O efeito sobre a farmacocinética de dutasterida em insuficiência hepática não foi estudado. No entanto, a exposição poderia ser maior em pacientes com insuficiência hepática porque dutasterida é extensamente metabolizada.
Tansulosina
A farmacocinética do cloridrato de tansulosina foi comparada em 8 indivíduos com disfunção hepática moderada (classificação de Child- Pugh: Graus A e B) e em 8 indivíduos normais. Embora se tenha observado uma mudança da concentração plasmática total do cloridrato de tansulosina como resultado da ligação alterada a AAG, a concentração não ligada (ativa) do cloridrato de tansulosina não mudou significativamente, apresentando alteração apenas moderada (32%) do clearance intrínseco do cloridrato de tansulosina não ligado. Portanto, os pacientes com disfunção hepática moderada não precisam de ajuste posológico de cloridrato de tansulosina. O cloridrato de tansulosina não foi estudado em pacientes com disfunção hepática grave.
Cuidados de Armazenamento
Conservar o produto em sua embalagem original e em temperatura ambiente (entre 15ºC e 30ºC).
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com prazo de validade vencido. Guarde-o em sua embalagem original.
Aspecto físico/características organolépticas
As cápsulas de Combodart são oblongas (ovaladas), duras, com corpo marrom e tampa laranja com a inscrição “GS 7CZ” impressa na cor preta.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
Dizeres Legais
MS: 1.0107.0287
Farm. Resp.:
Edinilson da Silva Oliveira
CRF-RJ Nº 18875
Fabricado por:
Catalent Germany Schorndorf GmbH
Steinbeisstrasse 2, D-73614 Schorndorf - Alemanha
Registrado e Importado por:
GlaxoSmithKline Brasil Ltda.
Estrada dos Bandeirantes, 8.464 - Rio de Janeiro - RJ
CNPJ: 33.247.743/0001-10
Venda sob prescrição médica.