Bula
Femoston 1 10 1Mg 1Mg 10Mg C 28 ComprimidosATENÇÃO: O texto abaixo deve ser utilizado apenas como uma referência secundária. É um registro histórico da bula, rótulo ou manual do produto. Este texto não pode substituir a leitura das informações que acompanha o produto, cujo fabricante podem mudar a formulação, recomendação, modo de uso e alertas legais sem que sejamos previamente comunicados. Apenas as informações contidas na própria bula, rótulo ou manual que acompanha o produto é que devem estar atualizadas de acordo com a versão comercializada porém, no caso de qualquer dúvida, consulte o serviço de atendimento ao consumidor do produto ou nossa equipe.
Bula - Femoston 1 10 1Mg 1Mg 10Mg C 28 Comprimidos
Para que serve
- Terapia Hormonal para mulheres com disfunções devido a menopausa natural ou cirurgicamente induzida.
- Prevenção da osteoporose pós-menopáusica.
- Terapia Hormonal para o alívio dos sintomas associados à deficiência estrogênica em mulheres com útero intacto. Prevenção da osteoporose pós-menopáusica em mulheres com útero intacto.
Contraindicação
- Em pacientes com carcinoma de mama conhecido , carcinoma endometrial ou outros tumores hormônio-dependentes.
- Doença hepática crônica ou aguda.
- História de doenças tromboembólicas venosas (por exemplo: trombose venosa profunda ou embolia pulmonar)
- Sangramento genital anormal.
- Gravidez ou suspeita de gravidez.
- Hipersensibilidade a qualquer um dos componentes da formulação.
Como usar
Uso Adulto
- Devem ser administrados por via oral, 1 compromido por dia sempre no mesmo horário.
- Durante os primeiros 14 dias consecutivos de um ciclo de 28 dias tomar um comprimido branco, e durante os 14 dias restantes tomar 1 comprimido cinza. Imediatamente após um ciclo de 28 dias, sem intervalos, iniciar o próximo ciclo de tratamento.
Precauções
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO História Médica e Exames Regulares O uso da Terapia de Reposição Hormonal (TRH) pode ter riscos que precisam ser considerados quando se decide iniciar o tratamento, ou continuar o tratamento A experiência em tratar mulher com menopausa prematura (devido a falha ovariana ou cirurgia) é limitada Se você teve uma menopausa prematura o risco de TRH pode ser diferente Por favor, converse com o seu médico Antes de iniciar (ou recomeçar a TRH), seu médico irá te perguntar sobre o seu histórico médico e o de sua família Seu médico pode decidir fazer um exame físico em você, que pode incluir um exame pélvico (genital) e de mamas, se necessário Uma vez inciado o tratamento com FEMOSTON® Conti você deve ir ao médico para exames regulares (pelo menos uma vez por ano) Nestes exames regulares, discuta com o seu médico os benefícios e riscos da continuação do tratamento com FEMOSTON® Conti Faça os exames de mama regularmente, como recomendado pelo seu médico Fale para o seu médico, antes de iniciar o tratamento, se você já teve qualquer um dos problemas a seguir Estes podem retonar ou piorar durante o tratamento com FEMOSTON® Conti Se isso acontecer, você deve procurar seu médico com mais frequência para realizar exames regulares • Mioma do seu útero; • Crescimento do revestimento do útero fora da cavidade uterina (endometriose) ou histórico de crescimento excessivo do revestimento do útero (hiperplasia endometrial); • Aumento do risco de desenvolver coágulos sanguíneos (doenças tromboembólicas) (ver “Coágulos de sangue na veia”); Femoston Conti_Bula_Paciente Abbott laboratórios do Brasil Ltda Rua Michigan 735, Brooklin São Paulo - SP CEP: 04566-905 Tel: 55 11 5536 7000 Fax: 55 11 5536 7126 • Aumento do risco de desenvolver câncer dependente de estrógenos (por exemplo: se tem uma irmã, mãe ou avó que tenha tido câncer de mama); • Pressão alta; • Desordens do fígado, como um tumor benigno de figado; • Diabetes; • Pedras na vesícula; • Enxaqueca ou dor de cabeça intensa; • Doença do sistema imunológico que afeta vários orgãos do corpo (Lupus eritematoso sistêmico - LES); • Epilepsia; • Asma; • Doença que afeta o tímpano e a audição (otosclerose); • Um altíssimo nível de gordura no sangue (triglicérides); • Retenção de líquidos, devido a problemas cardíaco ou renal (do rim) Razões para parar de tomar FEMOSTON® Conti imediatamente e procurar o seu médico:
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO História Médica e Exames Regulares O uso da Terapia de Reposição Hormonal (TRH) pode ter riscos que precisam ser considerados quando se decide iniciar , ou continuar o tratamento A experiência em tratar mulher com menopausa prematura (devido a falha ovariana ou cirurgia) é limitada Se você teve uma menopausa prematura o risco de TRH pode ser diferente Por favor, converse com o seu médico Antes de iniciar (ou recomeçar a TRH), seu médico irá te perguntar sobre o seu histórico médico e o de sua família Seu médico pode decidir fazer um exame físico em você, que pode incluir um exame pélvico (genital) e de mamas, se necessário Uma vez iniciado o tratamento com FEMOSTON® 1/10 você deve ir ao médico para exames regulares (pelo menos uma vez por ano) Nestes exames regulares, discuta com o seu médico os benefícios e riscos da continuação do tratamento com FEMOSTON® 1/10 Faça os exames de mama regularmente, como recomendado pelo seu médico Femoston_Bula_Paciente Abbott laboratórios do Brasil Ltda Rua Michigan 735, Brooklin São Paulo - SP CEP: 04566-905 Tel: 55 11 5536 7000 Fax: 55 11 5536 7126 Fale para seu médico, antes de iniciar o tratamento, se você já teve qualquer um dos problemas a seguir Estes podem retornar ou piorar durante o tratamento com FEMOSTON® 1/10 Se isso acontecer, você deve procurar seu médico com mais frequência para realizar exames regulares • Mioma do seu útero; • Crescimento do revestimento do útero fora da cavidade uterina (endometriose) ou histórico de crescimento excessivo do revestimento do útero (hiperplasia endometrial); • Aumento do risco de desenvolver coágulos sanguíneos (doenças tromboembólicas) (ver “Coágulos de sangue na veia”); • Aumento do risco de desenvolver câncer dependente de estrógenos (por exemplo: se tem uma irmã, mãe ou avó que tenha tido câncer de mama); • Pressão alta; • Desordem do fígado, como um tumor benigno de fígado; • Diabetes; • Pedras na vesícula; • Enxaqueca ou dor de cabeça intensa; • Doença do sistema imunológico que afeta vários órgãos do corpo (Lupus eritematoso sistêmico - LES); • Epilepsia; • Asma; • Doença que afeta o tímpano e a audição (otosclerose); • Um altíssimo nível de gordura no sangue (triglicérides); • Retenção de líquidos, devido a problemas cardíaco ou renal (do rim) Razões para parar de tomar FEMOSTON® 1/10 imediatamente e procurar o seu médico:
Reações Adversas
As reações adversas mais comumente reportadas pelas pacientes tratadas com estradiol/didrogesterona em estudos clínicos foram dor de cabeça, dor abdominal, dor/sensibilidade nas mamas e dor nas costas.
Os seguintes efeitos adversos foram observados com a frequência indicada abaixo durante estudos clínicos (n=4929):
Reações muito comuns (> 1/10)
Desordens do Sistema Nervoso
Dor de cabeça.
Desordens gastrointestinais
Dor abdominal.
Desordens do tecido conjuntivo e musculoesquelético
Dor nas costas.
Desordens do Sistema Reprodutivo e mama
Dor/sensibilidade aumentada nas mamas.
Reações comuns (? 1/100 e <1/10)
Infecções e infestações
Candidíase vaginal.
Desordens psiquiátricas
Depressão e nervosismo.
Desordens do Sistema Nervoso
Enxaqueca e tontura.
Desordens gastrointestinais
Náusea vômito e flatulência.
Desordens da pele e tecido subcutâneo
Reações alérgicas na pele (por exemplo: rash, urticária, prurido).
Desordens do Sistema Reprodutivo e mama
Desordens menstruais (incluindo metrorragia, menorragia, oligo/amenorreia, mestruação irregular, dismenorreia, sangramentos de escape, dor pélvica e secreção cervical).
Desordens gerais e alterações no local de administração
Condições de astenia (astenia, fatiga, indisposição) e edema periférico.
Investigações
Aumento de peso.
Reações incomuns (? 1/1.000 e <1/100)
Neoplasias benignas, malignas e não especificadas
Aumento no tamanho do leiomiomas.
Desordens do Sistema Imunológico
Hipersensibilidade.
Desordens psiquiátricas
Influência na libido.
Desordens vasculares
Tromboembolismo venoso (ver abaixo mais informações).
Desordens hepatobiliares
Função hepática anormal, ocasionalmente com icterícia, astenia ou mal-estar e dor abdominal, e desordens da vesícula biliar.
Desordens do sistema Reprodutivo e mamas
Aumento das mamas e síndrome pré-menstrual.
Investigações
Diminuição de peso.
Reações raras (? 1/10.000 e <1/1.000)
Desordens cardíacas
Infarto do miocárdio.
Desordens da pele e tecido subcutâneo
Angiodema, púrpura vascular.
Risco de câncer de mama
Um aumento de 2 vezes no risco de apresentar câncer de mama diagnosticado é reportado em mulheres que utilizaram terapia combinada de estrogênio e progestagênio por mais de 5 anos.
Qualquer aumento no risco de pacientes que utilizam a terapia de estrogênios isolados é substancialmente menor do que observado em pacientes que utilizam a terapia combinada de estrogênios e progestagênios.
O aumento de risco é dependente da duração do tratamento.
Resultados do principal estudo clínico randomizado e controlado por placebo (Estudo WHI) e o principal estudo epidemiológico (MWS) são apresentados a seguir.
Estudo MWS (Million Women Study) – Risco adicional estimado de câncer de mama após 5 anos de tratamento:

Estudo WHI (Womes’s Health Initiative) – Risco adicional de câncer de mama após 5 anos de tratamento
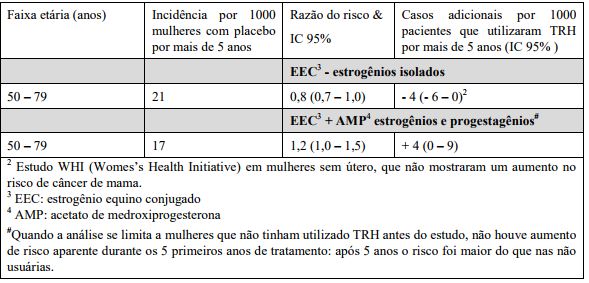
Risco de câncer endometrial (Mulheres pós-menopausa com útero intacto)
O risco de câncer endometrial é cerca de 5 em cada 1000 mulheres com útero intacto e que não utilizaram a TRH. Em mulheres com o útero intacto, o uso de TRH com estrogênios isolados não é recomendado porque este aumenta o risco de câncer endometrial. Dependendo da duração do tratamento e da dose utilizada de estrogênios isolados, o aumento de risco de câncer endometrial em estudos epidemiológicos, variou entre 5 e 55 casos diagnosticados a cada 1000 mulheres na faixa etária de 50 e 65 anos.
Adicionar um progestagênio à terapia com estrogênio isolado por no mínimo 12 dias por ciclo pode prevenir este risco aumentado. No estudo MWI o uso de TRH combinada (sequencial ou contínua) por 5 anos não aumentou o risco de câncer endometrial [RR de 1,0 (0,8 – 1,2)].
Câncer do ovário
O uso da TRH combinada ou com estrogênios isolados foi associado a um ligeiro aumento no risco de ter diagnóstico de câncer do ovário.
Uma meta-análise de 52 estudos epidemiológicos relataram um risco aumentado de câncer do ovário em mulheres que utilizam TRH comparado a mulheres que nunca utilizaram (RR 1,43, 95% IC 1,31 – 1,56). Para mulheres entre 50 e 54 anos com 5 anos de uso de TRH, isso resulta em cerca de 1 caso extra por 2000 usuárias. Em mulheres entre 50 e 54 anos que não estão utilizando TRH, cerca de 2 entre 2000 serão diagnosticadas com câncer de ovário ao longo de um período de 5 anos.
Risco de Tromboembolismo venoso
TRH está associada com um aumento de 1,3 a 3 vezes no risco de desenvolvimento de tromboembolismo venoso (TEV), ou seja, trombose venosa profunda ou embolismo pulmonar.
A ocorrência desses eventos é mais frequente entre no primeiro ano de uso da TRH. Os resultados dos estudos WHI são apresentados a seguir.
Estudo WHI (Womes’s Health Initiative) – Risco adicional de TEV após 5 anos de tratamento:
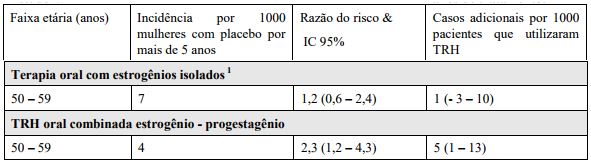
1 Estudo em mulheres sem útero.
Risco de Doença Arterial Coronariana
O risco de doença arterial coronariana é levemente aumentado em pacientes com 60 anos ou mais utilizando TRH combinada. Risco de Acidente Vascular Cerebral Isquêmico O uso da terapia combinada ou com estrogênios isolados está associado a um aumento de 1,5 vezes no risco de ataque isquêmico.
O risco de ataque hemorrágico não é aumentado durante o uso da TRH. O risco relativo não é dependente da idade ou da duração do tratamento, mas como o risco limiar é fortemente dependente da idade, o risco geral de ataque em mulheres que utilizam TRH aumentará com a idade.
Estudo WHI (Womes’s Health Initiative) combinado – Risco adicional de AVC isquêmico4 após 5 anos de tratamento:
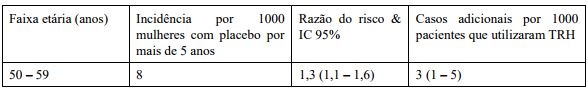 4 Nenhuma diferenciação foi feita entre acidente vascular cerebral isquêmico e hemorrágico.
4 Nenhuma diferenciação foi feita entre acidente vascular cerebral isquêmico e hemorrágico.
Outras reações adversas foram relatadas em associação ao tratamento com estrogênio / progestagênio (incluindo estradiol/didrogesterona):
Neoplasias benignas, malignas e não especificadas
Neoplasias dependentes de estrogênios tanto benignas quanto malignas, por exemplo, câncer endometrial e câncer ovariano. Aumento no tamanho de neoplasias dependentes de progestagênios, por exemplo: meningioma.
Desordens do sangue e sistema linfático
Anemia hemolítica.
Desordens do Sistema Imunológico
Lupus eritematoso sistêmico.
Desordens do metabolismo e nutrição
Hipertrigliceridemia.
Desordens do Sistema Nervoso
Provável demência, coreia e exacerbação da epilepsia.
Desordens oculares
Intolerância a lentes de contato e modificações na curvatura da córnea.
Desordens da pele e tecido subcutâneo
Eritema multiforme, eritema nodoso, cloasma ou melasma (que podem persistir quando o medicamento é descontinuado).
Desordens vasculares
Tromboembolismo arterial.
Desordens gastrointestinais
Pancreatite (em mulheres com hipertrigliceridemia pré-existente).
Desordens do tecido conjuntivo e musculoesquelético
Cãibras nas pernas.
Desordens renais e urinárias
Incontinência urinária.
Desordens do sistema Reprodutivo e mamas
Alterações fibrocísticas das mamas e erosão cervical uterina.
Desordens genéticas ou congênitas
Agravamento da porfiria.
Investigações
Aumento do hormônio tireoidiano total.
Em casos de eventos adversos, notifique à empresa e ao Sistema de Notificações em Vigilância Sanitária – NOTIVISA, disponível em www.anvisa.gov.br/hotsite/notivisa/index.htm, ou para a Vigilância Sanitária Estadual ou Municipal.
Composição
COMPOSIÇÃO Cada comprimido revestido salmão de FEMOSTON® Conti (estradiol + didrogesterona) contém: estradiol (17-beta-estradiol hemi-hidratado) 1,0 mg didrogesterona 5,0 mg Excipientes q s p 1 comprimido revestido Excipientes: lactose monoidratada, hipromelose, amido, dióxido de silício, estearato de magnésio, macrogol 400, dióxido de titânio, óxido de ferro amarelo e óxido de ferro vermelho II) INFORMAÇÕES À PACIENTE 1 PARA QUÊ ESTE MEDICAMENTO É INDICADO FEMOSTON® CONTI (estradiol + didrogesterona) é uma Terapia de Reposição Hormonal (TRH) que contém dois tipos de hormônios femininos, um estrogênio chamado estradiol e uma progesterona chamada didrogesterona FEMOSTON® Conti é indicado para mulheres que se encontram na pós menopausa (pelo menos 12 meses depois da sua última menstruação) FEMOSTON® Conti é utilizado para: ? Aliviar os sintomas ocorridos depois da menopausa Durante a menopausa, a quantidade de estrogênio produzido pela mulher diminui Isto pode causar sintomas como rosto, pescoço e peito quentes (ondas de calor) FEMOSTON® Conti alivia esses sintomas da menopausa FEMOSTON® Conti só será prescrito a você se os seus sintomas prejudicarem seriamente o seu dia a dia ? Prevenção da osteoporose Após a menopausa algumas mulheres podem desenvolver uma fragilidade nos ossos (osteoporose) Você deve discutir todas as opções disponíveis com seu médico Se você tem um alto risco de fraturas devido à osteoporose e outros medicamentos não são apropriados no seu caso, você pode usar FEMOSTON® Conti para prevenir a osteoporose após a menopausa 2
excipientes (ver “Composição”); • se você tem, teve ou se suspeita que tem câncer de mama; • se você tem ou se suspeita que tem câncer que é sensível ao estrogênio, tal como, câncer da mucosa do útero (câncer endometrial); • se você tem ou se suspeita que tem câncer que é sensível ao progestagênio, como por exemplo um tumor no cérebro (meningioma); • tem sangramento vaginal de causa desconhecida; • se você tem espessamento anormal da camada interna do útero (hiperplasia endometrial) para a qual você ainda não iniciou o tratamento; • se você tem ou teve um coágulo no vaso sanguíneo (tromboembolismo venoso), nas suas pernas (trombose venosa profunda) ou pulmões (embolia pulmonar); • se você tem uma desordem trombofílica (por exemplo: deficiência de proteína C, proteína S ou antitrombina III,); • se você tem ou teve recentemente uma doença causada por coágulos de sangue nas artérias (doença tromboembólica arterial), tais como angina, derrame ou ataque do coração (infarto do miocárdio); • tem ou se teve uma doença do fígado e seus valores no testes da função do fígado ainda não voltaram ao normal; • tem uma doença rara na pigmentação (coloração) do sangue chamada “porfiria” (alteração na produção de proteínas ligada ao pigmento dos glóbulos vermelhos), que pode ser de origem hereditária Se qualquer uma das condições acima aparecer pela primeira vez enquanto você estiver usando FEMOSTON® Conti, pare o tratamento e procure o seu médico imediatamente Este medicamento é contraindicado para uso por homens 4
COMPOSIÇÃO Cada comprimido revestido branco de FEMOSTON® 1/10 (estradiol/estradiol + didrogesterona) contém: estradiol (17-beta-estradiol hemi-hidratado) 1,0 mg Excipientes q s p 1 comprimido revestido Excipientes: lactose monoidratada, amido, dióxido de silício, estearato de magnésio, hipromelose, macrogol 400 e dióxido de titânio Cada comprimido revestido cinza de FEMOSTON® 1/10 (estradiol/ estradiol + didrogesterona) contém: estradiol (17-beta-estradiol hemi-hidratado) 1,0 mg didrogesterona 10,0 mg Excipientes q s p 1 comprimido revestido Excipientes: lactose monoidratada, amido, dióxido de silício, estearato de magnésio, hipromelose, álcool polivinílico, talco, macrogol 3350, dióxido de titânio e óxido de ferro preto II) INFORMAÇÕES À PACIENTE 1 PARA QUÊ ESTE MEDICAMENTO É INDICADO FEMOSTON® 1/10 (estradiol/ estradiol + didrogesterona) é uma Terapia de Reposição Hormonal (TRH) que contém dois tipos de hormônios femininos, um estrogênio chamado estradiol e uma progesterona chamanda didrogesterona FEMOSTON® 1/10 é indicado para mulheres que se encontram na perimenopausa, que não menstruam há pelo menos 6 meses, ou em mulheres na pós-menopausa FEMOSTON® 1/10 é utilizado para: ? Aliviar os sintomas ocorridos durante a menopausa Durante a menopausa, a quantidade de estrogênio produzido pela mulher diminui Isto pode causar sintomas como rosto, pescoço e peito quentes (ondas de calor) FEMOSTON® 1/10 alivia esses sintomas da menopausa FEMOSTON® 1/10 só será prescrito à você se os seus sintomas prejudicarem seriamente o seu dia a dia ? Prevenção da osteoporose Após a menopausa algumas mulheres podem desenvolver uma fragilidade nos ossos (osteoporose) Você deve discutir todas as opções disponíveis com seu médico Se você tem um alto risco de fraturas devido a osteoporose e outros medicamentos não são apropriados no seu caso, você pode usar FEMOSTON® 1/10 para prevenir a osteoporose após a menopausa Femoston_Bula_Paciente Abbott laboratórios do Brasil Ltda Rua Michigan 735, Brooklin São Paulo - SP CEP: 04566-905 Tel: 55 11 5536 7000 Fax: 55 11 5536 7126 2
excipientes (ver “Composição”); • se você tem, teve ou se suspeita que tem câncer de mama; • se você tem ou se suspeita que tem um câncer que é sensível ao estrogênio, tal como, câncer da mucosa do útero (câncer endometrial); • se você tem ou se suspeita que tem um câncer que é sensível a progestagênio, como por exemplo um tumor no cérebro (meningioma); • tem sangramento vaginal de causa desconhecida; • se você tem espessamento anormal da camada interna do útero (hiperplasia endometrial) para a qual você ainda não iniciou o tratamento; • se você tem ou teve um coágulo no vaso sanguíneo (tromboembolismo venoso), nas suas pernas (trombose venosa profunda) ou pulmões (embolia pulmonar); • se você tem uma desordem trombofílica (por exemplo: deficiência de proteína C, proteína S ou antitrombina III,); • se você tem ou teve recentemente uma doença causada por coágulos de sangue nas artérias (doença tromboembólica arterial), tais como angina, derrame ou ataque do coração (infarto do miocárdio); • tem ou se teve uma doença do fígado e seus valores no testes da função do fígado ainda não voltaram ao normal; • se você tem uma doença rara na pigmentação (coloração) do sangue chamada “porfiria” (alteração na produção de proteínas ligada ao pigmento dos glóbulos vermelhos), que pode ser de origem hereditária Se qualquer uma das condições acima aparecer pela primeira vez enquanto você estiver usando FEMOSTON® 1/10, pare o tratamento e procure o seu médico imediatamente Este medicamento é contraindicado para uso por homens 4
Interação Medicamentosa
Não foram realizados estudos de interação medicamentosa.
Casos em que a eficácia dos estrogênios e progestagênios pode ser prejudicada:
O metabolismo dos estrogênios pode ser aumentado pelo uso concomitante de substâncias que sabidamente induzem o aumento de enzimas metabolizadoras de medicamentos, especialmente enzimas P450, 2B6, 3A4, 3A5 e 3A7, tais como anticonvulsivantes (por exemplo: fenobarbital, carbamazepina, fenitoína) e anti-infecciosos (por exemplo: rifampicina, rifabutina, nevirapina, efavirenz).
Ritonavir e nelfinavir, embora reconhecidos como fortes inibidores do CYP450, 3A4, 3A5, 3A7, apresentam propriedades indutoras quando utilizados concomitantemente com hormônios esteróides.
Preparados contendo Erva de São João (Hypericum perforatum) podem induzir o metabolismo de estrogênios e progestagênios via CYP450, 3A4.
Clinicamente, o aumento do metabolismo de estrogênios e progestagênios podem levar a redução do efeito e mudanças no padrão de sangramento uterino.
Os estrogênios podem interferir com o metabolismo de outros fármacos:
Estrogênios, por si podem inibir as enzimas metabolizadoras de medicamentos CYP450 através da inibição competitiva. Isto é considerado particularmente para substratos com um índice terapêutico estreito, como: Tacrolimus e ciclosporina A (CYP450 3A4, 3A3); Fentanil (CYP450 3A4) Teofilina (CYP450 1A2).
Clinicamente isto pode levar a um aumento do nível plasmático das substâncias em questão até concentrações tóxicas. Portanto, o acompanhamento cuidadoso do medicamento por um longo período de tempo pode ser indicado, assim como uma diminuição da dose de tacrolimus, fentanil, ciclosporina A e teofilina podem ser necessários.
Ação da Substância
Resultados de Eficácia
Comprimidos Revestidos 1/10 mg
Alívio dos sintomas de deficiência de estrogênio e padrões de sangramento.
Alivio dos sintomas da menopausa foram alcançados durante as primeiras semanas de tratamento. Sangramento programado ocorreu em 76% das mulheres com a média de 5 dias de duração. A interrupção do sangramento normalmente começa na média no dia 28 do ciclo. Sangramento não programado (sangramento ou spotting de escape) apareceram em 23% das mulheres durante os primeiros 3 meses de terapia e em 15% das mulheres durante 10-12 meses de tratamento. Amenorreia (ausência de sangramento ou sangramento de escape) ocorreu em 21% dos ciclos durante o primeiro ano de tratamento.
Prevenção da osteoporose
A deficiência de estrôgenio na menopausa é associada com um aumento da perda de massa óssea. O efeito dos estrogênios na densidade mineral do osso é dose-dependente. A proteção parece ser efetiva pelo período que o tratamento é continuado. Depois da descontinuação da TRH, a taxa de perda de massa óssea é similar a de uma mulher que não faz terapia. Evidências dos resultados do estudo WHI e de dados de estudos de meta-análises mostram que o uso da TRH, isolada ou em combinação com progestagênio, causam predominantemente para as mulheres saudáveis, redução do risco de fratura osteoporótica de quadril, vértebras e outros. A TRH também previne fraturas em mulheres com baixa densidade óssea e/ou estabiliza osteoporose, mas as evidências são limitadas.
Para Estradiol + Didrogesterona (substância ativa) 1/10 (estradiol/ estradiol + didrogesterona) o aumento da densidade mineral óssea da coluna lombrar foi de 5,2% ± 3,8 (média ± DP), e a porcentagem de mulheres sem alteração no aumento da densidade mineral óssea na coluna lombar foi 93%. Estradiol + Didrogesterona (substância ativa) 1/10 também causou um efeito na densidade mineral óssea do quadril. Na região femural, o aumento depois de 2 anos de tratamento com Estradiol + Didrogesterona (substância ativa) 1/10 foi de 2,7% ± 4,2% (média ± DP) no colo femural, 3,5% ± 5,0% (média ± DP) no trocanter e 2,7% ± 6,7%(média ± DP) no triângulo de Wards. O percentual de mulheres que mantiveram o ganho de densidade mineral óssea nas 3 áreas do quadril depois do tratamento com Estradiol + Didrogesterona (substância ativa) 1/10 foi 67-78%.
Comprimidos Revestidos 1/5 mg
Alívio dos sintomas de deficiência de estrogênio e padrões de sangramento.
Alivio dos sintomas da menopausa foram alcançados durante as primeiras semanas de tratamento.
Amenorreia foi relatada por 88% das mulheres durante 10-12 meses de tratamento. Sangramento irregular ou sangramento não programado (sangramento ou spotting de escape) ocorreu em 15% das mulheres durante os primeiros 3 meses de tratamento e em 12% das mulheres durante 10-12 meses de tratamento.
Prevenção da osteoporose
A deficiência de estrôgenio na menopausa é associada com um aumento da perda de massa óssea. O efeito dos estrogênios na densidade mineral do osso é dose-dependente. A proteção parece ser efetiva pelo período que o tratamento é continuado. Depois da descontinuação da TRH, a taxa de perda de massa óssea é similar a de uma mulher que não faz terapia.
Evidências dos resultados do estudo WHI e de dados de estudos de meta-análises mostram que o uso da TRH, isolada ou em combinação com progestagênio, causam predominantemente para as mulher saudáveis, redução do risco de fratura osteoporótica de quadril, vértebras e outros.
A TRH também previne fraturas em mulheres com baixa densidade óssea e/ou estabiliza osteoporose, mas as evidências são limitadas. Depois de um ano de tratamento a densidade mineral óssea na coluna lombar aumentou cerca de 4,0% ± 3,4% (média ± DP). Em 90% dos sujeitos a densidade mineral óssea aumentou ou permaneceu a mesma durante o tratamento. FEMOSTON® Conti também causou um efeito na densidade mineral óssea do quadril. Na região femural, o aumento depois de um ano de tratamento foi de 1,5% ± 4,5% (média ± DP) no colo femural, 3,7% ± 6,0% (média ± DP) no trocanter e 2,1% ± 7,2% (média ± DP) no triângulo de Wards.
O percentual de mulheres que mantiveram o ganho de densidade mineral óssea nas 3 áreas do quadril depois do tratamento com FEMOSTON® Conti foi 71%, 66% e 81% respectivamente.2
Características Farmacológicas
O princípio ativo 17-beta-estradiol é química e biologicamente idêntico ao estradiol endógeno humano. O estradiol supre a diminuição da produção do estrogênio em mulheres na menopausa, aliviando os sintomas da menopausa. Os estrogênios previnem a perda óssea relacionada à menopausa ou em mulheres ooforectomizadas. A didrogesterona é um progestagênio oralmente ativo com atividade comparável à da progesterona administrada por via parenteral. Como os estrógenos promovem o crescimento do endométrio, estrógenos não opostos aumentam o risco de hiperplasia e câncer de endométrio. A adição de um progestagênio reduz significativamente o risco induzido por estrógenos de hiperplasia endometrial em mulheres não histerectomizadas.
Propriedades farmacocinéticas
Estradiol
Absorção:
A absorção do estradiol é dependente do tamanho da partícula, o estradiol micronizado é rapidamente absorvido pelo trato gastrointestinal. A tabela a seguir fornece a média dos parâmetros farmacocinéticos do estradiol (E2), estrona (E1), sulfato de estrona (E1S) para cada dose de estradiol micronizado no estado de equilíbrio. As informações estão apresentadas como média (DP).
Distribuição:
Os estrogênios podem ser encontrados tanto ligados quanto não ligados. Cerca de 98-99% da dose de estradiol se liga a proteínas plasmáticas, das quais cerca de 30-52% se ligam na albumina e cerca de 46-69% se ligam à globulina de hormônio sexual (SHBG).
Metabolismo:
Após a administração oral, o estradiol é extensivamente metabolizado. Os principais metabólitos conjugados e não conjugados são estrona e sulfato de estrona. Esses metabólitos podem contribuir para a atividade estrogênica diretamente, ou após a conversão em estradiol. O sulfato de estrona pode passar pela circulação êntero-hepática.
Eliminação:
Na urina os principais componentes são os glicuronídeos da estrona e estradiol. A meiavida de eliminação está entre 10-16h. Os estrogênios são excretados no leite materno.
Dependência de dose e tempo:
Após administração oral diária de Estradiol + Didrogesterona (substância ativa) , as concentrações de estradiol atingiram o estado de equilíbrio em 5 dias. Geralmente, as concentrações no estado de equilíbrio parecem ser alcançados entre 8 a 11 dias de administração.
Comprimidos Revestidos 1/10
Propriedades farmacocinéticas — Didrogesterona
Absorção:
Após administração oral, a didrogesterona é rapidamente absorvida com Tmáx entre 0,5 e 2,5 horas. A biodisponibilidade absoluta da didrogesterona (oral em dose de 20 mg x 7,8 mg de infusão intravenosa) é de 28%. A tabela a seguir fornece os parâmetros farmacocinéticos médios da didrogesterona (D) e da diidrodidrogesterona (DHD) após alcançar o estado de equilíbrio. As informações estão apresentadas como média (DP).
|
Didrogesterona 10mg | ||
|
Parâmetros | D | DHD |
|
Cmáx (ng/mL) | 2,54 (1,80) |
62,50 (33,10) |
|
Cmin (ng/mL) | 0,13 (0,07) |
3,70 (1,67) |
|
Cav (ng/mL) | 0,42 (0,25) |
13,04 (4,77) |
|
AUC0-t (ng.h/mL) | 9,14 (6,43 |
311,17 (114,35) |
Distribuição:
Após administração intravenosa de didrogesterona o volume de distribuição no estado de equilíbrio é de aproximadamente 1400L. Didrogesterona e DHD estão mais que 90% ligadas às proteínas plasmáticas.
Metabolismo:
Após a administração oral, a didrogesterona é rapidamente metabolizada à DHD. Os níveis de pico do principal metabólito ativo 20-alfa-diidrodidrogesterona (DHD) estão cerca de 1,5 h após a administração. Os níveis plasmáticos de DHD são substancialmente maiores quando comparados com a droga precursora. As razões de AUC e Cmáx de DHD para didrogesterona estão na ordem de 40 e 25, respectivamente. A média da meias-vida terminal da didrogesterona e DHD variam entre 5 a 7 horas e de 14 a 17 horas, respectivamente. Uma característica comum de todos os metabólitos identificados é a conservação da configuração 4,6 dieno-3-ona da droga percusora e a ausência da 17-alfa-hidroxilação. Isto explica a ausência de efeitos estrogênicos e androgênicos da didrogesterona.
Eliminação:
Após a administração oral de didrogesterona marcada, em média 63% da dose é excretada pela urina. A depuração plasmática total é de 6,4 L/min, sendo a excreção completa em 72 horas. A DHD está presente na urina principalmente como um ácido glicurônico conjugado. Dependência de dose e tempo: doses farmacocinéticas simples ou múltiplas são lineares em uma dose oral entre 2,5 e 10 mg. A comparação da cinética da dose simples e de múltiplas doses mostra que a farmacocinética da didrogesterona e da DHD não são alteradas como um resultado de doses repetidas. O estado de equilíbrio foi alcançado após 3 dias de tratamento.
Comprimidos Revestidos 1/5
Propriedades farmacocinéticas — Didrogesterona
Absorção:
Após administração oral, a didrogesterona é rapidamente absorvida com Tmáx entre 0,5 e 2,5 horas. A biodisponibilidade absoluta da didrogesterona (oral em dose de 20 mg x 7,8 mg de infusão intravenosa) é de 28%.
A tabela a seguir fornece os parâmetros farmacocinéticos médios da didrogesterona (D) e da diidrodidrogesterona (DHD) após alcançar o estado de equilíbrio. As informações estão apresentadas como média (DP).
|
Didrogesterona 5mg | ||
|
Parâmetros | D | DHD |
| Cmax (ng/mL) | 0,90 | 24,68 |
|
AUCinf (ng*h/mL) | 1,55 (1,08) | 98,37 |
|
AUC0-t (ng.h/mL | - | 121,36 (63,63) |
Distribuição:
Após administração intravenosa de didrogesterona o volume de distribuição no estado de equilíbrio é de aproximadamente 1400L. Didrogesterona e DHD estão mais que 90% ligadas às proteínas plasmáticas.
Metabolismo:
Após a administração oral, a didrogesterona é rapidamente metabolizada à DHD. Os níveis de pico do principal metabólito ativo 20-alfa-diidrodidrogesterona (DHD) estão cerca de 1,5 h após a administração. Os níveis plasmáticos de DHD são substancialmente maiores quando comparados com a droga precursora. As razões de AUC e Cmáx de DHD para didrogesterona estão na ordem de 40 e 25, respectivamente. A média da meias-vida terminal da didrogesterona e DHD variam entre 5 a 7 horas e de 14 a 17 horas, respectivamente. Uma característica comum de todos os metabólitos identificados é a conservação da configuração 4,6 dieno-3-ona da droga percusora e a ausência da 17-alfa-hidroxilação. Isto explica a ausência de efeitos estrogênicos e androgênicos da didrogesterona.
Eliminação:
Após a administração oral de didrogesterona marcada, em média 63% da dose é excretada pela urina. A depuração plasmática total é de 6,4 L/min, sendo a excreção completa em 72 horas. A DHD está presente na urina principalmente como um ácido glicurônico conjugado.
Dependência de dose e tempo:
Doses farmacocinéticas simples ou múltiplas são lineares em uma dose oral entre 2,5 e 10 mg. A comparação da cinética da dose simples e de múltiplas doses mostra que a farmacocinética da didrogesterona e da DHD não são alteradas como um resultado de doses repetidas. O estado de equilíbrio foi alcançado após 3 dias de tratamento.
Cuidados de Armazenamento
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO FEMOSTON® Conti (estradiol + didrogesterona) deve ser mantido em sua embalagem original Conservar em temperatura ambiente entre 15°C e 30ºC Número de lote e datas de fabricação e validade: vide embalagem Não use medicamento com o prazo de validade vencido Guarde-o em sua embalagem original FEMOSTON® Conti (estradiol + didrogesterona) é apresentado em cartelas com 28 comprimidos revestidos de cor salmão, redondos e biconvexos Antes de usar, observe o aspecto do medicamento Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo Todo medicamento deve ser mantido fora do alcance das crianças 6
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO FEMOSTON® 1/10 (estradiol/estradiol + didrogesterona) deve ser mantido em sua embalagem original Conservar em temperatura ambiente entre 15°C e 30ºC Número de lote e datas de fabricação e validade: vide embalagem Não use medicamento com o prazo de validade vencido Guarde-o em sua embalagem original FEMOSTON® 1/10 (estradiol/ estradiol + didrogesterona) é composto por comprimidos revestidos com duas cores diferentes, é apresentado em cartelas com 14 comprimidos brancos (para os primeiros 14 dias Femoston_Bula_Paciente Abbott laboratórios do Brasil Ltda Rua Michigan 735, Brooklin São Paulo - SP CEP: 04566-905 Tel: 55 11 5536 7000 Fax: 55 11 5536 7126 do ciclo) e 14 comprimidos cinza (para os próximos 14 dias do ciclo)cada Cada cartela contém 28 comprimidos Cada comprimido branco contém 1 mg de 17-beta-estradiol e cada comprimido cinza contém 1 mg de 17-beta-estradiol + 10 mg de didrogesterona que estão sob a forma de comprimidos revestidos, redondos e biconvexos Antes de usar, observe o aspecto do medicamento Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo Todo medicamento deve ser mantido fora do alcance das crianças 6
Dizeres Legais
III) DIZERES LEGAIS: Registro M S : 1 0553 0349 Farmacêutico responsável: Ana Paula Antunes Azevedo CRF-RJ nº 6572 Fabricado por: Abbott Biologicals B V Olst – Holanda Importado por: Abbott Laboratórios do Brasil Ltda Rio de Janeiro - RJ INDÚSTRIA BRASILEIRA Femoston Conti_Bula_Paciente Abbott laboratórios do Brasil Ltda Rua Michigan 735, Brooklin São Paulo - SP CEP: 04566-905 Tel: 55 11 5536 7000 Fax: 55 11 5536 7126 Registrado por: Abbott Laboratórios do Brasil Ltda Rua Michigan, 735 São Paulo – SP CNPJ: 56 998 701/0001-16 ABBOTT CENTER Central de Relacionamento com o Cliente 0800 703 1050 www abbottbrasil com br VENDA SOB PRESCRIÇÃO MÉDICA Femoston Conti_Bula_Paciente Abbott Laboratórios do Brasil Ltda Rua Michigan 735, Brooklin São Paulo - SP CEP: 04566-905 Tel: 55 11 5536 7000 Fax: 55 11 5536 7126 Histórico de alterações do texto de bula Número do expediente Nome do assunto Data da notificação/ petição Data de aprovação da petição Itens alterados 0270663/13-6 10458 - MEDICAMENTO NOVO - Inclusão Inicial de Texto de Bula – RDC 60/12 10/04/2013 10/04/2013 1a submissão 0710035/13-3 10451 - MEDICAMENTO NOVO – Notificação de Alteração de Texto de Bula – RDC 60/12
III) DIZERES LEGAIS: Registro M S : 1 0553 0349 Farmacêutico responsável: Ana Paula Antunes Azevedo CRF-RJ nº 6572 Fabricado por: Abbott Biologicals B V Olst – Holanda Importado por: Abbott Laboratórios do Brasil Ltda Rio de Janeiro - RJ INDÚSTRIA BRASILEIRA Registrado por: Abbott Laboratórios do Brasil Ltda Rua Michigan, 735 São Paulo – SP CNPJ: 56 998 701/0001-16 BU21 ABBOTT CENTER Central de Relacionamento com o Cliente 0800 703 1050 www abbottbrasil com br VENDA SOB PRESCRIÇÃO MÉDICA Femoston_Bula_Paciente Abbott Laboratórios do Brasil Ltda Rua Michigan 735, Brooklin São Paulo - SP CEP: 04566-905 Tel: 55 11 5536 7000 Fax: 55 11 5536 7126 Histórico de alterações do texto de bula Número do expediente Nome do assunto Data da notificação/ petição Data de aprovação da petição Itens alterados 0270663/13-6 10458 - MEDICAMENTO NOVO - Inclusão Inicial de Texto de Bula – RDC 60/12 10/04/2013 10/04/2013 1a submissão 0710035/13-3 10451 - MEDICAMENTO NOVO – Notificação de Alteração de Texto de Bula – RDC 60/12 26/08/2013 26/08/2013 Sem alteração 10451 - MEDICAMENTO NOVO – Notificação de Alteração de Texto de Bula – RDC 60/12 18/09/2013 18/09/2013 1 PARA QUÊ ESTE MEDICAMENTO É INDICADO 4 O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO 6 COMO DEVO USAR ESTE MEDICAMENTO 7 O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO 9 O QUE FAZER SE ALGUÉM USAR UMA GRANDE QUANTIDADE DESTE MEDICAMENTO DE UMA SÓ VEZ Femoston_Bula_Paciente_Histórico 1
