Bula
Rasilez - 300Mg 28 ComprimidosATENÇÃO: O texto abaixo deve ser utilizado apenas como uma referência secundária. É um registro histórico da bula, rótulo ou manual do produto. Este texto não pode substituir a leitura das informações que acompanha o produto, cujo fabricante podem mudar a formulação, recomendação, modo de uso e alertas legais sem que sejamos previamente comunicados. Apenas as informações contidas na própria bula, rótulo ou manual que acompanha o produto é que devem estar atualizadas de acordo com a versão comercializada porém, no caso de qualquer dúvida, consulte o serviço de atendimento ao consumidor do produto ou nossa equipe.
Bula - Rasilez - 300Mg 28 Comprimidos
Para que serve
Rasilez é indicado para tratar a pressão arterial alta.
A pressão arterial alta aumenta a carga de trabalho do coração e das artérias.
A permanência da pressão arterial em níveis elevados por um longo período pode danificar os vasos sanguíneos do cérebro, coração e rins, podendo resultar em acidente vascular cerebral, insuficiência cardíaca, ataque cardíaco e insuficiência renal.
A pressão arterial alta aumenta o risco de ataques cardíacos. A redução da pressão arterial a níveis normais diminui o risco de desenvolvimento desses problemas.
Como o Rasilez funciona?
Antes de usar Rasilez, leia atentamente esta bula. Você deve guardá-la com você, pois pode ser necessário utilizá-la novamente.
Não dê seu medicamento para mais ninguém usar e não use este medicamento para tratar qualquer outra doença para qual este medicamento não é indicado.
Seu medicamento chama-se Rasilez e está disponível na forma de comprimidos revestidos. Cada comprimido contém 150 mg ou 300 mg da substância ativa alisquireno.
O alisquireno pertence a uma nova classe de medicamentos chamada de inibidores da renina que ajudam a reduzir a pressão alta.
Os inibidores da renina reduzem a quantidade de angiotensina II que o corpo produz. A angiotensina II causa um estreitamento dos vasos sanguíneos, o que aumenta a pressão sanguínea. A redução da quantidade de angiotensina II permite que os vasos sanguíneos relaxem, o que leva a uma redução da pressão sanguínea.
Se você tiver alguma dúvida sobre como Rasilez funciona ou porque este medicamento foi prescrito para você, pergunte ao seu médico.
Contraindicação
- Se você for alérgico (hipersensível) ao Rasilez ou a qualquer um dos seus componentes mencionados nesta bula. Se você acha que pode ser alérgico, fale com seu médico;
- Se você tem diabetes tipo 2 (também chamada de diabetes mellitus não dependente de insulina) e se você está tomando um tipo especial de medicação chamada bloqueador dos receptores de angiotensina (BRA) ou inibidor das enzimas conversoras de angiotensina (IECA) ao mesmo tempo;
- Se o paciente é menor de dois anos de idade.
Se qualquer dessas situações se aplicarem a você, avise ao seu médico e não tome Rasilez. O seu médico irá decidir se este medicamento é adequado para você.
Se você acha que pode ser alérgico, solicite informações ao seu médico.
Como usar
Siga cuidadosamente as instruções do seu médico. Não exceda a dose recomendada.
Pacientes com pressão arterial alta frequentemente não percebem os sinais desse problema. Muitos pacientes se sentem normais. É muito importante que você tome esse medicamento exatamente como seu médico lhe recomendou para alcançar os melhores resultados e reduzir o risco de reações adversas.
Mantenha suas consultas com seu médico mesmo se você estiver se sentindo bem.
Quando e como tomar Rasilez
Os comprimidos de Rasilez devem ser engolidos inteiros com uma pequena quantidade de água.
Não mastigue ou esmague os comprimidos.
Os comprimidos podem ser tomados com ou sem comida.
Quanto tomar de Rasilez
Normalmente a dose inicial é de um comprimido revestido de 150 mg uma vez ao dia. Em alguns casos, seu médico pode prescrever uma dose mais alta (p. ex.: comprimido revestido de 300 mg) ou um medicamento adicional para tratar a pressão arterial alta.
Seu médico dirá a você exatamente quantos comprimidos de Rasilez você deve tomar. Dependendo da sua resposta ao tratamento, seu médico pode sugerir uma dose maior ou menor.
Por quanto tempo tomar Rasilez?
Siga exatamente as instruções de seu médico. Ele dirá a você por quanto tempo você deverá tomar Rasilez.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento.
Não interrompa o tratamento sem o conhecimento do seu médico.
Este medicamento não pode ser partido ou mastigado.
O que devo fazer quando eu me esquecer de tomar o Rasilez?
Se você esquecer-se de tomar uma dose, tome-a assim que você se lembrar. Se estiver quase na hora da sua próxima dose, você deve simplesmente tomar o próximo comprimido no horário normal.
Não tome uma dose dobrada para compensar a dose perdida.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
Precauções
Siga cuidadosamente todas as orientações de seu médico. Elas podem diferir das informações gerais contidas nesta bula.
O seu médico pode desejar fazer um exame de sangue antes e em intervalos regulares durante o seu tratamento, para verificar os valores de potássio, magnésio, cálcio, sódio, açúcar, colesterol, ácido úrico e as quantidades de glóbulos vermelhos e brancos, assim como as plaquetas.
Seu médico também pode monitorar a sua função renal.
Tome cuidado especial com Rasilez
- Se você tiver a função renal comprometida com sintomas como redução da eliminação de urina (ou outras condições que possam impactar na função renal) ou um estreitamento ou bloqueio da artéria que conduz sangue ao rim. Isso é especialmente importante se você está tomando outros medicamentos que afetem o sistema renina-angiotensina-aldosterona (SRAA) ou certos tipos de analgésicos chamados Anti-Inflamatórios Não Esteroidais (AINEs). Seu médico poderá verificar seus níveis sanguíneos de eletrólitos (principalmente potássio) e também sua função renal;
- Se você está tomando um diurético (medicamento que aumenta a quantidade de urina que você produz) ou medicamentos utilizados para controlar a pressão arterial que agem no sistema renina-angiotensina-aldosterona (SRAA), tais como BRAs ou IECAs;
- Se você está grávida ou está planejando engravidar;
- Se você estiver tomando ciclosporina (medicamento usado após transplante para prevenir a rejeição de órgão ou para outras condições, como por exemplo: artrite reumatoide ou dermatite atópica) ou itraconazol (medicamento usado para tratar infecções fúngicas).
Se qualquer dessas situações se aplica a você, avise seu médico antes de tomar Rasilez.
Se você apresentar pressão arterial baixa no começo do tratamento, consulte seu médico.
Durante o tratamento, pare de tomar Rasilez e contate o seu médico imediatamente se você tiver
- Dificuldade para respirar ou engolir;
- Aperto no peito;
- Urticária;
- Erupção cutânea;
- Inchaço;
- Coceira;
- Tontura;
- Vômitos;
- Dor abdominal (sinais de uma reação alérgica grave);
- Inchaço, sobretudo da face e garganta (sinal de angioedema).
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Reações Adversas
Como ocorre com todos os medicamentos, os pacientes tomando Rasilez podem apresentar algumas reações adversas, embora nem todas as pessoas as apresentem.
Rasilez pode causar as seguintes reações adversas graves
Pressão arterial baixa (hipotensão)
Sua pressão arterial pode cair muito se você também toma medicamentos diuréticos, está sob dieta restritiva de sal, está em tratamento de diálise, tem problemas cardíacos ou sente-se mal, com vômitos ou diarreia.
Repouse se você sentir fraqueza ou tontura.
Entre em contato com seu médico imediatamente.
Algumas reações adversas podem ser sérias (frequência desconhecida)
- Reação alérgica (hipersensibilidade) com sintomas como erupções cutâneas, coceira, urticária, dificuldade em respirar ou engolir, tontura, vômito, dor abdominal (isso pode ser sinal de uma reação alérgica grave, chamada de reação anafilática);
- Se você desenvolver uma reação alérgica envolvendo inchaço da face, lábios, garganta e/ou língua que possa causar dificuldade de respirar e de engolir (angioedema), pare de tomar Rasilez e entre em contato com seu médico imediatamente;
- Erupção cutânea, pele avermelhada, formação de bolhas nos lábios, olhos ou boca, descamação da pele, febre (pode ser sinal de uma condição chamada necrólise epidérmica tóxica ou síndrome de Stevens-Johnson);
- Disfunção renal com sintomas tais como redução severa da eliminação de urina ou redução da eliminação de urina. Estes podem ser sintomas de insuficiência renal ou falência renal;
- Náuseas, perda do apetite, urina escurecida ou amarelamento da pele e dos olhos (sinais de distúrbios hepáticos).
Se você apresentar qualquer um destes sintomas, informe ao seu médico imediatamente.
Outras reações adversas
Reações adversas comuns (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento)
- Diarreia;
- Níveis elevados de potássio no sangue (hiperpotassemia).
Reações adversas incomuns (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento)
- Erupção cutânea;
- Tosse.
Reações adversas com frequência desconhecida
- Coceira;
- Vermelhidão da pele;
- Tontura;
- Edema, levando ao inchaço das mãos, tornozelo ou pés;
- Pressão arterial baixa;
- Náusea;
- Vômito;
- Testes da função do fígado anormais;
- Testes da função dos rins anormais;
- Resultados de exames de sangue anormais;
- Baixo nível de células no sangue;
- Baixo nível de sódio no sangue.
Se alguma dessas reações adversas afetarem você gravemente, ou se você notar quaisquer reações adversas não descritas acima, por favor, avise ao seu médico ou farmacêutico.
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também à empresa através do seu serviço de atendimento.
População Especial
Idosos (65 anos ou mais)
Você pode tomar Rasilez se você tiver 65 anos de idade ou mais.
Crianças e adolescentes (menores de 18 anos)
Rasilez deve ser somente utilizado por adultos.
É contraindicado em pacientes com menos de 2 anos de idade e não deve ser utilizado em pacientes de 2 anos a menos de 6 anos de idade.
Rasilez não é recomendado para pacientes entre 6 anos e menores de 18 anos de idade.
Gravidez e amamentação
Este medicamento pertence à categoria de risco na gravidez C (primeiro trimestre) e D (segundo e terceiro trimestres).
Rasilez não deve ser utilizado por mulheres grávidas ou que possam ficar grávidas durante o tratamento. Se você engravidar, pare de tomar Rasilez e avise seu médico imediatamente.
Se você planeja engravidar, converse com seu médico sobre outras opções de tratamento para pressão arterial alta.
Avise seu médico se você está amamentando. Você não deve amamentar se estiver tomando Rasilez, pois pode ser prejudicial ao bebê.
Este medicamento não deve ser utilizado por mulheres grávidas ou que possam ficar grávidas durante o tratamento.
Efeitos na habilidade de dirigir e operar máquinas
Nenhum estudo de efeitos sobre a habilidade de dirigir e operar máquinas foi conduzido.
A eficácia deste medicamento depende da capacidade funcional do paciente.
Composição
Cada comprimido revestido de Rasilez 150 mg contém
165,750 mg de hemifumarato de alisquireno (equivalente a 150 mg de alisquireno).
Cada comprimido revestido de Rasilez 300 mg contém
331,500 mg de hemifumarato de alisquireno (equivalente a 300 mg de alisquireno).
Excipientes: celulose microcristalina, crospovidona, povidona, estearato de magnésio, dióxido de silício, macrogol, talco, hipromelose, dióxido de titânio, óxido férrico vermelho e óxido férrico preto.
Superdosagem
Se você tomar acidentalmente muitos comprimidos, consulte seu médico imediatamente. Você pode precisar de uma atenção médica.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
Interação Medicamentosa
Interações farmacodinâmicas
Anti-inflamatórios não esteroidais (AINEs) incluindo inibidores seletivos da cicloxigenase-2 (inibidores da COX-2):
Em pacientes idosos com depleção de volume (incluindo aqueles em tratamento com diuréticos), ou com função renal comprometida, a coadministração de AINEs com os agentes que atuam no sistema renina-angiotensina-aldosterona pode resultar na deterioração da função renal, incluindo possível falência renal aguda, que geralmente é reversível. A administração concomitante com AINEs pode atenuar o efeito anti-hipertensivo dos agentes que atuam no sistema renina-angiotensina-aldosterona, incluindo o alisquireno.
Potássio e diuréticos poupadores de potássio:
Baseado na experiência com o uso de outros medicamentos que afetam o sistema renina-angiotensina-aldosterona, o uso concomitante do alisquireno com os seguintes medicamentos pode levar ao aumento do potássio sérico: diuréticos poupadores de potássio, suplementos de potássio, ou sais substitutos contendo potássio. Deve-se ter cautela se a coadministração for considerada necessária.
Duplo bloqueio do sistema renina-angiotensina-aldosterona (SRAA):
O uso concomitante de alisquireno com outros fármacos com ação sobre o SRAA, tais como IECAs ou BRAs, está associado a um aumento do risco de hipotensão, hiperpotassemia, e alterações na função renal (incluindo falência renal aguda) em comparação com a monoterapia.
Recomenda-se monitorar a pressão arterial, a função renal e os eletrólitos em pacientes que fazem uso de alisquireno e outros agentes que afetam o SRAA.
O uso concomitante de alisquireno com um BRA ou um IECA em pacientes com diabetes tipo 2 é contraindicado e deve ser evitado em pacientes com função renal gravemente comprometida.
Furosemida:
A coadministração oral de furosemida e alisquireno não teve nenhum efeito sobre a farmacocinética do alisquireno, mas reduziu a exposição à furosemida. Quando o alisquireno (300 mg/dia) foi coadministrado com furosemida oral (20 mg/dia) em indivíduos saudáveis, a ASC e o Cmáx da furosemida foram reduzidos em 28% e 49%, respectivamente. Em pacientes com insuficiência cardíaca, a coadministração do alisquireno (300 mg/dia) reduziu o ASC e Cmáx plasmáticos da furosemida oral (60 mg/dia) em 17% e 27%, respectivamente, e reduziu a excreção urinária de furosemida no período de 24 horas em 29%.
Durante a coadministração de alisquireno (300 mg/dia) e furosemida (60 mg/dia), a excreção urinária de sódio e o volume de urina foram reduzidos durante as primeiras 4 horas em 31% e 24%, respectivamente, em comparação apenas com a furosemida. Pequenas modificações na farmacocinética e eficácia da furosemida foram observadas com alisquireno 150 mg/dia, que não alcançaram significância estatística.
Nenhuma diferença estatisticamente significativa no volume total de urina e excreção urinária de sódio durante 24 horas foi observada no estado de equilíbrio quando a furosemida foi administrada isoladamente em comparação com a coadministração com alisquireno 150 mg ou 300 mg.
Não houve alteração estatisticamente significativa no peso dos pacientes tratados concomitantemente com furosemida e alisquireno (média = 83,6 kg com 150 mg de alisquireno e média = 84,6 kg com 300 mg de alisquireno) em relação ao peso corporal dos pacientes tratados com furosemida isoladamente (média = 83,4 kg). Em pacientes tratados com furosemida oral e alisquireno, é recomendado que os efeitos da furosemida sejam monitorados quando se inicia ou se ajusta a dose de furosemida ou alisquireno.
Interações farmacocinéticas
Hemifumarato De Alisquireno possui um baixo potencial de interações farmacocinéticas com outros medicamentos.
Os compostos que foram investigados nos estudos clínicos farmacocinéticos incluíram acenocumarol, atenolol, celecoxibe, fenofibrato, pioglitazona, alopurinol, mononitrato de isossorbida-5, irbesartana, digoxina, ramipril e hidroclorotiazida, e nenhuma interação foi identificada.
A coadministração com irbesartana reduziu a Cmáx do alisquireno em até 50% após doses múltiplas. A coadministração de alisquireno com valsartana (redução de 28%), metformina (redução de 28%), anlodipino (aumento de 29%) ou cimetidina (aumento de 19%), resultou em uma alteração na Cmáx ou ASC de alisquireno entre 20% e 30%. Quando administrado com atorvastatina, o estado de equilíbrio de alisquireno e sua ASC e Cmáx aumentaram em 50%.
A coadministração de alisquireno não teve nenhum impacto significante na farmacocinética da atorvastatina, valsartana, metformina ou anlodipino. Como resultado, não é necessário nenhum ajuste de dose para alisquireno ou para esses medicamentos coadministrados. No entanto, é necessário cautela no uso concomitante de alisquireno com BRA ou IECA.
Interações com glicoproteína P (Pgp):
Estudos in vitro indicam que a MDR1 (Pgp) foi achada como sendo a principal transportadora de efluxo envolvida na absorção e disposição do alisquireno. O potencial de interações medicamentosas no sítio da Pgp dependerá provavelmente do grau de inibição deste transportador.
Inibidores potentes de Pgp:
Um estudo de interação medicamentosa com dose única em sujeitos saudáveis tem mostrado que a ciclosporina (200 e 600 mg) aumenta a Cmáx de alisquireno 75 mg por aproximadamente 2,5 vezes e a ASC por aproximadamente 5 vezes. Em indivíduos saudáveis, itraconazol (100 mg) aumenta a ASC e Cmáx de alisquireno (150 mg) em 6,5 e 5,8 vezes, respectivamente. Portanto, o uso concomitante desses medicamentos com alisquireno não é recomendado.
Inibidores moderados de Pgp:
A coadministração de cetoconazol (200 mg) com alisquireno (300 mg) resultou em um aumento de 80% das concentrações plasmáticas de alisquireno (ASC e Cmáx). Estudos pré-clínicos indicaram que a coadministração de alisquireno e cetoconazol intensifica a absorção gastrintestinal de alisquireno e diminui a excreção biliar. A coadministração de uma dose oral única de 300 mg de alisquireno com 240 mg de verapamil aumentou a ASC e Cmáx de alisquireno em aproximadamente 2 vezes.
Espera-se que a alteração nas concentrações plasmáticas de alisquireno na presença de cetoconazol ou verapamil seja dentro da faixa que seria atingida se a dose de alisquireno fosse dobrada; doses de alisquireno até 600 mg, ou duas vezes a maior dose terapêutica recomendada, têm sido relatada como bem tolerada em estudos clínicos controlados. Como resultado, o ajuste de dose do alisquireno não é necessário.
Substratos Pgp ou inibidores fracos:
Nenhuma interação relevante com atenolol, digoxina, anlodipino e cimetidina foi observada.
Quando administrado com atorvastatina (80 mg), a ASC e a Cmáx do alisquireno (300 mg) no estado de equilíbrio aumentaram 50%.
Interações com a CYP450:
O alisquireno não inibe as isoenzimas CYP450 (CYP1A2, 2C8, 2C9, 2C19, 2D6, 2E1 e CYP3A). O alisquireno não induz a CYP3A4. O alisquireno é minimamente metabolizado pelas enzimas do citocromo P450, portanto não é esperado que o alisquireno afete a exposição sistêmica de substâncias que inibam, induzam ou sejam metabolizadas por essas enzimas.
Varfarina:
Os efeitos do alisquireno sobre a farmacocinética da varfarina não foram avaliados em estudos clínicos bem controlados.
Ação da Substância
Resultados da eficácia
Hipertensão
Em pacientes hipertensos, Hemifumarato De Alisquireno (substância ativa) causa uma redução prolongada dose-dependente em ambas as pressões sistólica e diastólica. Há um aumento na resposta em todas as doses administradas, com efeitos razoáveis observados entre 150 e 300 mg, mas não há aumento adicional claro quando é administrada uma dose de 600 mg. A administração de Hemifumarato De Alisquireno (substância ativa) uma vez ao dia em doses de 150 mg e 300 mg forneceram uma redução efetiva na pressão arterial durante o intervalo completo de 24 horas (mantendo-se benéfico no início da manhã), com uma relação vale-pico média para resposta diastólica de 98% para a dose de 300 mg.
Após duas semanas, 85 a 90% do efeito na redução da pressão arterial máxima foram observados. O efeito na redução da pressão arterial foi mantido em pacientes tratados por até um ano como demonstrado por uma diferença estatisticamente significante com o placebo 4 semanas após a retirada randomizada. Com a cessação do tratamento, a pressão arterial retornou gradualmente aos seus níveis basais no período de algumas semanas, sem evidência de um efeito rebote da pressão arterial ou da APR.
O alisquireno reduziu a pressão arterial em todos os subgrupos demográficos, embora os pacientes negros tendessem a ter uma redução menor do que caucasianos e asiáticos, conforme observado com inibidores da ECA e bloqueadores do receptor de angiotensina (BRAs).
Não há evidências de hipotensão na dose inicial e de nenhum efeito na frequência cardíaca dos pacientes tratados nos estudos controlados. A hipotensão excessiva foi incomum (0,1%) em pacientes com hipertensão não complicada tratados somente com Hemifumarato De Alisquireno (substância ativa).Hipotensão também foi incomum (< 1%) durante a terapia combinada com outros agentes anti-hipertensivos.
Em estudos controlados, o efeito na redução da pressão arterial de Hemifumarato De Alisquireno (substância ativa) em combinação com hidroclorotiazida ou ramipril foi aditivo e as combinações foram bem toleradas. A combinação de Hemifumarato De Alisquireno (substância ativa) com o ramipril (inibidor da ECA) reduziu a incidência de tosse quando comparado ao ramipril administrado isoladamente (alisquireno/ramipril 1,8% vs. ramipril 4,7%).
Hemifumarato De Alisquireno (substância ativa) 150 mg também teve um efeito aditivo na redução da pressão arterial e foi bem tolerado em pacientes que não responderam adequadamente à dose de 5 mg de anlodipino (bloqueador do canal de cálcio). A eficácia foi semelhante à alcançada com 10 mg de anlodipino, mas houve uma menor incidência de edema (alisquireno/anlodipino 2,1% vs. anlodipino 11,2%). A coadministração com a valsartana (BRA) foi bem tolerada.
A eficácia na redução da pressão arterial de Hemifumarato De Alisquireno (substância ativa) é comparada a outras classes de agentes anti-hipertensivos incluindo os inibidores da enzima conversora de angiotensina I (IECAs), bloqueadores de receptor de angiotensina (BRAs) e bloqueadores de canais de cálcio (BCCs).
O efeito anti-hipertensivo de Hemifumarato De Alisquireno (substância ativa) e da hidroclorotiazida (HCTZ) foi comparado em um estudo de grupo paralelo, duplo-cego, randomizado de 26 semanas com opção adicional de anlodipino. Após 12 semanas de monoterapia com alisquireno 300 mg e HCTZ 25 mg, a redução da pressão arterial (sistólica/diastólica) basal foi 17,0/12,3 mmHg para alisquireno e 14,4/10,5 mmHg para HCTZ. No término do estudo, a redução da pressão arterial (sistólica/diastólica) basal foi 19,6/14,2 mmHg com alisquireno 300 mg e 17,9/13,0 mmHg com HCTZ 25 mg.
Em pacientes hipertensos diabéticos, a monoterapia com Hemifumarato De Alisquireno (substância ativa) foi segura e efetiva. Em combinação com ramipril, Hemifumarato De Alisquireno (substância ativa) promoveu uma redução da pressão arterial adicional comparada com os componentes em monoterapia.
A adição de Hemifumarato De Alisquireno (substância ativa) ao tratamento de pacientes hipertensos obesos não controlados com hidroclorotiazida promoveu uma redução adicional da pressão arterial, comparável à promovida pela adição de irbesartana ou anlodipino.
Os efeitos anti-hipertensivos de Hemifumarato De Alisquireno (substância ativa) foram independentes da idade, sexo, índice de massa corpórea e raça.
Em um estudo de 3 meses realizado com 302 pacientes com atual diagnóstico ou histórico de hipertensão e insuficiência cardíaca estável leve, os quais estavam recebendo terapia padrão para insuficiência cardíaca estável (inibidor da ECA ou BRA, um betabloqueador e para um terço dos pacientes um antagonista da aldosterona), a adição de Hemifumarato De Alisquireno (substância ativa) 150 mg foi bem tolerada. Os níveis do peptídeo natriurético tipo B (PNB) foram reduzidos em 25% no braço Hemifumarato De Alisquireno (substância ativa) em comparação ao braço placebo.
A eficácia e segurança da terapia baseada em alisquireno foram comparadas com terapia baseada em ramipril em um estudo de nove meses com 901 pacientes idosos (? 65 anos) com hipertensão sistólica essencial. Alisquireno 150 mg ou 300 mg por dia ou ramipril 5 mg ou 10 mg por dia foram administrados por 36 semanas, com opcional terapia concomitante adicional de hidroclorotiazida (12,5 mg ou 25 mg) na semana 12, e anlodipino (5 mg ou 10 mg) na semana 22. Durante o período de 12 semanas, a monoterapia com alisquireno reduziu a pressão arterial sistólica / diastólica em 14,0/5,1 mmHg, em comparação com 11,6/3,6 mmHg para ramipril. As diferenças em ambas as pressões sistólica e diastólica foram estatisticamente significativas. Após 12 semanas, 46,3% dos pacientes necessitaram de tratamento concomitante com a hidroclorotiazida no regime com alisquireno, em comparação com 55,5% dos pacientes tratados em regime baseado em ramipril. Após 22 semanas 11,5% dos pacientes necessitaram de tratamento concomitante com o anlodipino no regime com alisquireno em comparação com 15,7% dos pacientes tratados com ramipril.
A tolerabilidade foi semelhante em ambos os grupos de tratamento, no entanto a tosse foi mais frequentemente relatada no tratamento com ramipril do que com o tratamento com alisquireno (14,2% vs 4,4%). A reação adversa mais comum para o tratamento com alisquireno foi diarreia (6,6% vs 5,0% para o tratamento com ramipril).
Em um estudo duplo-cego, randomizado, ativo-controlado, em que a eficácia foi avaliada em 1.181 pacientes, a administração única diária de alisquireno 300 mg com anlodipino 10 mg e HCTZ 25 mg, produziu reduções estatisticamente significantes na pressão arterial média (sistólica/diastólica) de 37,9/20,6 mmHg em comparação a 31,4/18,0 mmHg com a combinação alisquireno/anlodipino (300/10 mg), 28,0/14,3 mmHg com alisquireno/hidroclorotiazida (300/25 mg) e 30,8/17,0 mmHg com anlodipino/hidroclorotiazida (10/25 mg) em pacientes com hipertensão moderada a grave.
Em pacientes com hipertensão grave (PAS ? 180 mmHg), a redução da pressão arterial para a combinação tripla de alisquireno, HCTZ e anlodipino foi 49,5/22,5 mmHg em comparação a 38,1/17,6 mmHg com a combinação alisquireno/amlodipino (300/10 mg), 33,2/14,3 mmHg com alisquireno/hidroclorotiazida (300/25 mg) e 39,9/17,8 mmHg com anlodipino/hidroclorotiazida (10/25 mg). A combinação de alisquireno/anlodipino/HCTZ foi geralmente bem tolerada e a reação adversa mais comumente relatada foi edema periférico.
A segurança e tolerabilidade gastrintestinal (GI) a longo prazo do alisquireno foi avaliada em um estudo de 54 semanas, randomizado, duplo-cego, ativo controlado (ramipril), em pacientes com hipertensão essencial, de pelo menos, 50 anos de idade. Não houve diferença estatisticamente significante no risco relativo no desfecho composto ou qualquer um de seus componentes (pólipos hiperplásicos, pólipos inflamatórios, pólipos adenomatosos e carcinoma), como avaliado por colonoscopia, após um ano de tratamento com alisquireno 300 mg por dia em comparação com ramipril 10 mg por dia, com um risco relativo total de 1,03. A duplicação do risco relativo de desfecho composto (resultado primário do estudo) foi excluída com p < 0,0001. Os índices de hiperplasia da mucosa, displasia e a gravidade da inflamação foram baixos no início e os aumentos não foram observados em nenhum dos dois grupos de tratamento. Nenhum efeito patológico de alisquireno no cólon ou reto foi detectado.
Pacientes pediátricos
A eficácia de alisquireno em pacientes pediátricos hipertensos de 6 a 17 anos de idade foi avaliada em um estudo de 8 semanas no qual a dose-resposta foi avaliada na fase inicial de 4 semanas, randomizada, duplo-cega, e os pacientes então continuaram em uma fase de retirada de 4 semanas, duplo-cega, randomizada, para avaliação futura da eficácia de alisquireno comparada ao placebo. Na fase de dose-resposta inicial, 267 pacientes foram randomizados para os grupos de dose baixa, média e alta de alisquireno.

No final do período de tratamento de 4 semanas, o alisquireno reduziu a pressão arterial sistólica e diastólica de um modo dependente da dose.
O alisquireno reduziu significativamente a pressão arterial sistólica em 4,8, 5,6 e 8,7 mmHg a partir da linha de base nos grupos de dose baixa, média e alta, respectivamente. Os pacientes foram então re-randomizados ou para continuar na mesma dose de alisquireno ou para serem transferidos para o placebo durante mais 4 semanas. No final de 4 semanas dessa segunda fase, a pressão sanguínea sistólica dos pacientes tratados com alisquireno coincidiu com a pressão arterial sistólica observada em pacientes transferidos para o placebo para todos os grupos de doses (baixo, p = 0,889; médio, p = 0,951; alta, p = 0,056).
A média das diferenças na pressão arterial sistólica média entre alisquireno e placebo para os grupos de doses baixa, média e alta, foram -0,2, -0,1 e -2,7 mmHg, respectivamente.
Subsequente ao estudo de 8 semanas, 208 pacientes pediátricos hipertensos de 6 a 17 anos de idade entraram em um estudo de extensão de 52 semanas no qual os pacientes foram randomizados para receber alisquireno ou enalapril. O estudo de extensão incluiu 3 níveis de dose com base no peso. As titulações opcionais da dose foram autorizadas durante o estudo para controlar a pressão arterial.
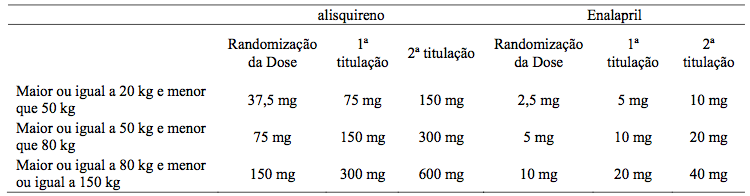
No final de 52 semanas, as reduções na pressão arterial sistólica em relação à linha de base foram semelhantes em pacientes tratados com alisquireno (7,63 mmHg) e enalapril (7,94 mmHg), com um p-valor = 0,004 não inferior. Não houve diferenças estatisticamente significativas entre alisquireno (-3,90 mmHg) e enalapril (-4,94 mmHg) em relação à alterações da linha de base até o final do estudo para a pressão arterial diastólica (p = 0,3187).
O tratamento com alisquireno foi bem tolerado nesses estudos.
Características Farmacológicas
Classe farmacoterapêutica: inibidor de renina.
Código ATC: C09XA02.
Mecanismo de ação
Hemifumarato De Alisquireno (substância ativa) é um inibidor direto seletivo e potente, não peptídico, ativo oralmente, da renina humana. Hemifumarato De Alisquireno (substância ativa) atinge o sistema renina-angiotensina-aldosterona (SRAA) no ponto de ativação por ligação à enzima renina, bloqueando a conversão de angiotensinogênio em angiotensina I e reduzindo os níveis de atividade plasmática de renina (APR), angiotensina I e angiotensina II.
Farmacodinâmica
A renina é secretada pelo rim em resposta à redução no volume sanguíneo e na perfusão renal. Essa resposta inicia um ciclo que inclui o sistema renina-angiotensina-aldosterona (SRAA) e um ciclo de realimentação homeostático. A renina cliva o angiotensinogênio formando o decapeptídeo inativo, a angiotensina I (Ang I). A Angiotensina I é convertida em um octapeptídeo ativo, a angiotensina II (Ang II), pela enzima conversora de angiotensina (ECA) e também por vias não ECA dependentes. A Angiotensina II é um potente vasoconstritor e promove a liberação de catecolaminas da medula adrenal e das terminações nervosas pré-juncionais. Ela também estimula a secreção de aldosterona e a reabsorção de sódio. Juntos, esses efeitos aumentam a pressão arterial. O aumento crônico de Angiotensina II resulta em uma expressão de marcadores e mediadores da inflamação e fibroses associados com o dano de órgãos alvo. A Ang II também inibe a liberação de renina, fornecendo, assim, uma reação negativa ao sistema. A atividade da renina plasmática (ARP) elevada foi independentemente associada ao aumento do risco cardiovascular em pacientes hipertensos e normotensos.
Todos os agentes que inibem este sistema, incluindo inibidores da renina, suprimem o ciclo de realimentação negativo, conduzindo a um aumento compensatório na concentração da renina plasmática. Quando esse aumento ocorre durante o tratamento com inibidores da ECA e bloqueadores de receptores de angiotensina (BRAs, ele é acompanhado de aumento da atividade plasmática da renina (APR). Entretanto, durante o tratamento com alisquireno, os efeitos do ciclo de realimentação são neutralizados. Como resultado, APR, Ang I, e Ang II são todas reduzidas, quando alisquireno é usado como monoterapia ou em combinação com outros agentes anti-hipertensivos.
O tratamento com Hemifumarato De Alisquireno (substância ativa) reduz a APR em pacientes hipertensos. Nos estudos clínicos, as reduções da APR variaram aproximadamente de 50 a 80%. Não foram relacionados com a dose e não se correlacionam com reduções da pressão arterial. As implicações clínicas das diferenças no efeito sobre a APR não são conhecidas. Reduções similares foram observadas quando o alisquireno foi combinado com outros medicamentos anti-hipertensivos.
Os efeitos do alisquireno nos outros componentes do SRAA, por exemplo, nas vias ECA e não ECA, não são conhecidos.
Farmacocinética
Absorção
Após absorção oral, o pico das concentrações plasmáticas de alisquireno é alcançado depois de 1 a 3 horas. A biodisponibilidade absoluta de alisquireno é 2,6%. A alimentação reduz o Cmax e a exposição (ASC), mas tem um impacto mínimo sobre a farmacodinâmica, portanto, pode ser administrada sem respeitar a alimentação. Quando administrado com uma refeição rica em gordura, a ASC média e a Cmáx do alisquireno foram reduzidas em 71% e 85%, respectivamente. Nos estudos clínicos, o alisquireno foi administrado sem exigir uma relação fixa com as refeições. As concentrações plasmáticas no estado de equilíbrio são alcançadas em aproximadamente 5 a 7 dias se administrado uma vez ao dia e os níveis no estado de equilíbrio são aproximadamente duas vezes maiores que os obtidos com a dose inicial.
Transportadores
Em estudos pré-clínicos a MDR1/Mdr1a/1b (Pgp) foi encontrada ser o principal sistema de efluxo envolvido na absorção intestinal e excreção biliar de alisquireno.
Distribuição
O alisquireno é distribuído de maneira sistêmica e uniforme após a administração oral.
Após administração intravenosa, o volume médio de distribuição no estado de equilíbrio é de aproximadamente 135 L, indicando que o alisquireno se distribui extensivamente no espaço extravascular. A ligação às proteínas plasmáticas é moderada (47 a 51%) e independente de sua concentração.
Metabolismo e eliminação
A meia-vida de eliminação é de aproximadamente 40 horas (variando de 34 a 41 horas). O alisquireno é eliminado principalmente como um composto inalterado nas fezes (78%).
Aproximadamente 1,4% da dose oral total é metabolizada. A enzima responsável pela metabolização é a CYP3A4. Aproximadamente 0,6% da dose é recuperada na urina após administração oral. Após administração intravenosa, o clearance (depuração) plasmático médio é de aproximadamente 9 L/h.
Linearidade/não linearidade
O pico das concentrações plasmáticas (Cmáx) e a exposição (ASC) de alisquireno aumentam linearmente com o aumento da dose no intervalo de 75 a 600 mg.
População especial
Hemifumarato De Alisquireno (substância ativa) é um tratamento anti-hipertensivo efetivo administrado uma vez ao dia em pacientes adultos, independente do sexo, idade, índice de massa corpórea e raça.
Insuficiência renal
A farmacocinética do alisquireno foi avaliada em pacientes com variados níveis de insuficiência renal. A ASC relativa e a Cmáx de alisquireno em indivíduos com insuficiência renal variaram entre 0,8 a duas vezes quando comparados aos indivíduos sadios após a administração de uma dose única e no estado de equilíbrio. Porém, essas alterações observadas não estão correlacionadas com a gravidade da insuficiência renal. Não é necessário nenhum ajuste de dose inicial de Hemifumarato De Alisquireno (substância ativa) em pacientes com insuficiência renal leve a moderada. O uso de Hemifumarato De Alisquireno (substância ativa) não é recomendado em pacientes com insuficiência renal grave (TFG < 30 mL/min).
A farmacocinética do alisquireno foi avaliada em pacientes com Doença Renal em Estágio Terminal (DRET) submetidos à hemodiálise. A administração de uma dose oral única de 300 mg de alisquireno foi associada com pequenas alterações na farmacocinética de alisquireno (alteração no Cmáx de menos de 1,2 vezes; aumento da ASC de até 1,6 vezes) em comparação com indivíduos saudáveis pareados. O tempo de hemodiálise não alterou significativamente a farmacocinética de alisquireno em pacientes com DRET. Portanto, nenhum ajuste da dose é justificado em pacientes com DRET submetidos à hemodiálise.
Insuficiência hepática
A farmacocinética do alisquireno não foi significativamente afetada em pacientes com doença hepática leve a grave. Consequentemente, não é necessário nenhum ajuste na dose inicial de Hemifumarato De Alisquireno (substância ativa) em pacientes com insuficiência hepática leve a grave.
Pacientes idosos (com 65 anos ou mais)
Não é necessário ajuste de dose inicial de Hemifumarato De Alisquireno (substância ativa) para pacientes idosos.
Pacientes pediátricos
A farmacocinética do alisquireno foi avaliada em um estudo farmacocinético de 8 dias com 39 pacientes pediátricos hipertensos de 6 a 17 anos de idade. O alisquireno foi administrado em doses diárias de 2 mg/kg ou 6 mg/kg, na forma de minicomprimidos (3,125 mg/minicomprimido). Os parâmetros farmacocinéticos do alisquireno foram similares aos observados nos adultos, e os resultados deste estudo não sugerem que a idade, o peso corporal ou o sexo tenham qualquer efeito significativo sobre a exposição sistêmica de alisquireno.
Em um estudo duplo-cego, randomizado, de 8 semanas com alisquireno em monoterapia em 267 pacientes pediátricos hipertensos de 6 a 17 anos de idade, as concentrações mínimas em jejum de alisquireno no Dia 28 demonstraram níveis mínimos de exposição à droga comparáveis aos observados em outros estudos utilizando doses semelhantes de alisquireno, tanto em adultos como em crianças. Neste estudo, existem 3 grupos de doses de alisquireno administradas de acordo com o peso.
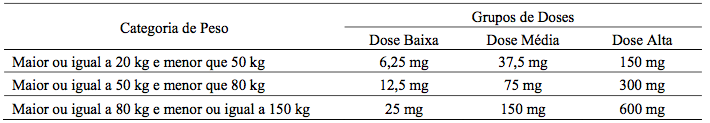
Os resultados de um estudo in vitro de MDR1 (Pgp) no tecido humano sugeriu uma idade e tecido padrão dependente da maturação de MDR1. A alta variabilidade interindividual dos níveis de expressão de mRNA foi observada (até 600 vezes). Expressão hepática MDR1 mRNA foi significativamente menor nas amostras de fetos, recém-nascidos e bebês de até 23 meses.
A idade em que MDR1 (Pgp) está madura não pode ser determinada. Existe um potencial de superexposição para o alisquireno em crianças com MDR1 imaturo.
Dados de segurança pré-clínicos
Carcinogenicidade
O potencial carcinogênico foi avaliado em um estudo de 2 anos em ratos e de 6 meses em camundongos transgênicos. Nenhum potencial carcinogênico foi detectado. Alterações inflamatória e proliferativa foram observadas no trato gastrintestinal inferior com doses de 750 ou 1.500 mg/kg/dia em ambas as espécies. Embora não haja aumentos estatisticamente significantes na incidência de tumor associado com a exposição ao alisquireno, foi observada hiperplasia da mucosa epitelial (com ou sem erosão/ulceração) no trato gastrintestinal inferior em doses de 750 ou mais mg/kg/dia nas duas espécies, com um adenoma de cólon identificado em um rato e um adenocarcinoma cecal, identificado em outro, tumores raros nas espécies de ratos estudados.
Com base na exposição sistêmica (ASC0-24h), 1.500 mg/kg/dia em ratos é aproximadamente 4 vezes, e em camundongos aproximadamente 1,5 vezes, a dose máxima humana recomendada (300 mg alisquireno/dia). A hiperplasia da mucosa do ceco ou do cólon nos ratos também foi observada em doses orais de 250 mg/kg/dia (a dose mais baixa testada) assim como nas doses mais altas em 4 e 13 semanas de estudo. Concentrações fecais locais na dose de nível de não evento adverso 250 mg/kg/dia em estudos de carcinogenicidade em ratos foram 16 a 24 vezes mais altas que no homem, na maior dose clínica recomendada de 300 mg. Os resultados de um estudo de toxicidade oral subsequente de 104 semanas em macacos saguis mostram a ausência de qualquer mudança histopatológica no trato gastrintestinal relacionada ao tratamento com doses de 10 e 20 mg/kg/dia. Margens de segurança obtidas em humanos na dose de 300 mg foram 9 – 11 vezes baseadas em concentrações fecais ou em 6 vezes baseadas em concentrações na mucosa, em comparação ao nível de não evento adverso de 250 mg/kg/dia no estudo de carcinogenicidade em ratos.
Mutagenicidade
O alisquireno foi isento de qualquer potencial mutagênico em estudos in vitro e in vivo de mutagenicidade. Os estudos incluíram ensaios in vitro em bactérias e células de mamíferos e in vivo, avaliações em ratos.
Toxicidade reprodutiva
Estudos de toxicidade reprodutiva com alisquireno não revelaram qualquer evidência de toxicidade embriofetal ou teratogenicidade com doses de até 600 mg/kg/dia em ratos ou 100 mg/kg/dia em coelhos. Doses de até 250 mg/kg/dia não afetaram a fertilidade e o desenvolvimento pré e pós-natal de ratos. As doses em ratos e coelhos foram 6 – 16 e 6 vezes, respectivamente, a dose máxima recomendada para humanos (300 mg) com base em mg/m2 (cálculos considerando um paciente com 50 kg).
Estudos em animais jovens
Estudos de toxicidade em ratos jovens indicaram que a exposição excessiva de alisquireno (> 400 vezes maior em ratos com 8 dias de idade, em comparação com ratos adultos) e a toxicidade associada são causadas por MDR1 imatura. Isto sugere que, em pacientes pediátricos com MDR1 imatura, há um potencial para a superexposição de alisquireno e toxicidade associada.
Cuidados de Armazenamento
Você deve guardar este medicamento em temperatura ambiente (entre 15 e 30ºC), na embalagem original. Proteger da umidade.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Aspecto físico
Rasilez 150 mg
Comprimido revestido rosa claro, redondo e biconvexo, impresso “IL” em uma face e “NVR” em outra.
Rasilez 300 mg
Comprimido revestido vermelho claro, oval e biconvexo, impresso “IU” em uma face e “NVR” em outra.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Mensagens de Alerta
Todo medicamento deve ser mantido fora do alcance das crianças.
Dizeres Legais
MS – 1.0068.1055
Farm. Resp.: Flavia Regina Pegorer – CRF-SP 18.150
Importado por:
Novartis Biociências S.A.
Av. Prof. Vicente Rao, 90
São Paulo - SP
CNPJ: 56.994.502/0001-30
Indústria Brasileira
Fabricado por: Novartis Pharma Stein AG, Stein, Suíça e/ou Novartis Farma S.p.A., Torre Annunziata, Itália.
Venda sob prescrição médica.
Esta bula foi aprovada pela Anvisa em 01/02/2016.