para o que é indicado e para que serve?
Para que serve - É indicado no tratamento das crises agudas de enxaqueca, acompanhada ou não de distúrbios visuais, sensitivos ou de vômitos.Continue lendo...
ofertas de
Sutriptan - 50 Mg 2 Compr...
ofertas de Sutriptan - 50 Mg 2 Compr...
ATENÇÃO: O texto abaixo deve ser utilizado apenas como uma referência secundária. É um registro histórico da bula, rótulo ou manual do produto. Este texto não pode substituir a leitura das informações que acompanha o produto, cujo fabricante podem mudar a formulação, recomendação, modo de uso e alertas legais sem que sejamos previamente comunicados. Apenas as informações contidas na própria bula, rótulo ou manual que acompanha o produto é que devem estar atualizadas de acordo com a versão comercializada porém, no caso de qualquer dúvida, consulte o serviço de atendimento ao consumidor do produto ou nossa equipe.
Para que serve
- É indicado no tratamento das crises agudas de enxaqueca, acompanhada ou não de distúrbios visuais, sensitivos ou de vômitos.
- A forma injetável é indicada para o tratamento da cefaléia . Não deve ser usada como profilático.
Contraindicação
- Hipersensibilidade a qualquer dos componentes da fórmula.
- Pacientes com isquemia cardíaca, infarto do miocárdio preexistente ou angina, hipertensão não controlada, enxaqueca, pacientes sob tratamento com inibidores da monoaminoxidase, com inibidores seletivos da recaptação 5- HT serotonina ou com lítio.
Como usar
Uso Oral ou Injetável.
- A dose recomendada para adultos é de 6 mg (0,5 ml) por injeção subcutânea.
- Comprimidos revestidos: a dose recomendada é de 1 comprimido de 100 mg de sumatriptana. Nos casos em que os sintomas persistam, ou retornem, até 3 comprimidos podem ser administrados em 24 horas, sempre com, no mínimo, 3 horas entre cada administração.
Precauções
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO Se você responder SIM a qualquer uma das perguntas abaixo, avise seu médico ANTES de usar este medicamento: - Você está grávida ou tentando engravidar - Você está amamentando - Esta crise de enxaqueca é diferente das que você está acostumado a ter - Já lhe disseram que você é alérgico à sumatriptana ou a qualquer outro componente de SUTRIPTAN®
Reações Adversas
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR
Como todo medicamento, SUTRIPTAN® pode causar reações adversas Algumas pessoas podem ser alérgicas a determinadas medicações Se você sentir algum dos seguintes sintomas logo após usar SUTRIPTAN®, PARE de usar este medicamento e avise seu médico imediatamente: falta de ar repentina ou aperto no peito; inchaço nas pálpebras, face ou lábios; convulsão; erupções cutâneas em qualquer parte do corpo; dor abdominal ou sangramento retal Dados de estudos clínicos Reações comuns (ocorrem entre 1% e 10% dos pacientes que utilizam este medicamento): tonteira, sonolência; aumentos transitórios da pressão sanguínea, aparecendo logo após o tratamento; rubor (vermelhidão da face por um curto período de tempo); dificuldade para respirar; sensação de náusea ou vômito; sensação de calor ou frio; sensação de peso ou pressão em qualquer parte do corpo, incluindo peito e garganta; sensação de fraqueza e cansaço (normalmente temporários e de intensidade leve a moderada); dor ou sensação de dormência Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento): pequenas alterações nos testes para avaliar a função do fígado foram observados ocasionalmente Dados pós-comercialização Reações muito raras (ocorrem em menos de 0,01% dos pacientes que utilizam este medicamento): reações alérgicas, variando de hipersensibilidade cutânea à anafilaxia, que são reações alérgicas graves e generalizadas; convulsões; tremores; movimentos descontrolados; distúrbios visuais, como visão tremida, reduzida, dupla, perda de visão e, em alguns casos, alterações permanentes (embora esses distúrbios possam ocorrer devido à crise de enxaqueca); batimentos do coração mais lentos ou mais rápidos que o normal, ou sensação de batimentos cardíacos irregulares ou fortes; palidez nos dedos dos pés e das mãos (fenômeno de Raynaud); pressão sanguínea baixa; colite isquêmica Se algum destes sintomas ocorrer, você não precisa parar de tomar o medicamento, mas avise seu médico na próxima consulta Entretanto, caso você apresente uma coloração roxa persistente dos pés e das mãos, pare de tomar o medicamento e avise seu médico imediatamente Se você experimentar uma dessas reações ou qualquer reação adversa não descrita nesta bula, por favor, informe seu médico Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento Informe também à empresa através do seu serviço de atendimento 9 O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO Se você acidentalmente exceder a dose máxima diária permitida, contate seu médico imediatamente Leve a embalagem e a bula com você, para que ele possa identificar o que está tomando 5 Em caso de uso de uma grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível Ligue para 0800 722 6001, se você precisar de mais orientações
Composição
COMPOSIÇÃO Cada comprimido revestido com 50 mg contém: succinato de sumatriptana (equivalente a 50 mg de sumatriptana)* 70 mg *Excipientes: celulose microcristalina, croscarmelose sódica, estearato de magnésio, lactose Cada comprimido revestido com 100 mg contém: succinato de sumatriptana (equivalente a 100 mg de sumatriptana)* 140 mg Excipientes: celulose microcristalina, croscarmelose sódica, estearato de magnésio, lactose, óxido de ferro vermelho 30 II - INFORMAÇÕES AO PACIENTE 1
(ver “Composição”) - Você está usando medicamentos que contenham ergotamina ou diidroergotamina Caso esteja, não use SUTRIPTAN® ao mesmo tempo - Você faz uso, ou fez uso nas últimas duas semanas, de antidepressivos, particularmente aqueles chamados inibidores da monoaminoxidase (IMAO) ou inibidores seletivos de recaptação de serotonina (ISRS) Se a resposta for positiva, você não deve utilizar SUTRIPTAN® - Você é alérgico a antibióticos à base de sulfonamidas Se você é alérgico a algum tipo de antibiótico, mas não tem certeza se ele pertence a esse grupo, consulte seu médico - Você é portador de colite isquêmica (inflamação no intestino grosso devido à redução da circulação sanguínea) - Você apresenta falta de ar, dor ou aperto no peito (que pode ou não se espalhar para o maxilar ou braços) - Você já teve um ataque cardíaco - Você tem pressão alta - Você tem algum problema cardíaco ou sofre de angina - Você já teve, ou lhe foi dito que pode vir a ter, um acidente vascular cerebral (AVC) ou um ataque isquêmico transitório (AIT) - Você tem doença de Raynaud (contração das pequenas artérias das mãos e pés, com redução da circulação), doença vascular periférica (DVP) dos membros inferiores (dor atrás das pernas) ou apresenta dormência ou pontadas nas mãos e nos pés - Já lhe disseram que você tem alto risco de vir a ter problemas no coração Considere-se como propenso a ter doença no coração caso você: seja homem com mais de 40 anos; seja mulher que já está na menopausa; seja obeso; tenha diabetes; tenha níveis elevados de colesterol; seja fumante; tenha histórico na família - Você tem doença no fígado - Você tem doença no rim - Você já teve ataques epilépticos ou convulsões no passado Já lhe disseram que você possui propensão a ter esses problemas Este medicamento é de uso exclusivamente oral SUTRIPTAN® comprimidos revestidos só deve ser utilizado quando houver um diagnóstico claro de enxaqueca Use este medicamento conforme prescrição médica As doses recomendadas não devem ser excedidas A administração concomitante de qualquer triptano/agonista do receptor 5-HT1 com SUTRIPTAN® não é recomendada O abuso de SUTRIPTAN® pode estar associado ao agravamento da dor Caso seja esse o seu caso, procure seu médico, pois pode ser necessário suspender o tratamento Efeitos sobre a capacidade de dirigir veículos e operar máquinas SUTRIPTAN® ou a própria enxaqueca pode fazer com que você se sinta sonolento Portanto, não é recomendado que você dirija veículos ou opere máquinas, caso esteja tendo uma crise 3 Gravidez e lactação O uso de SUTRIPTAN® não é recomendado durante a gravidez Se você está grávida, ou pretende engravidar, não use SUTRIPTAN® sem consultar seu médico Ele vai avaliar os benefícios esperados para você em comparação aos riscos do uso de SUTRIPTAN® para o feto Os componentes de SUTRIPTAN® podem passar pelo leite materno Por isso, não amamente seu bebê com seu leite por até 12 horas após fazer uso de SUTRIPTAN® Caso você produza leite durante esse período, retire-o e descarte-o Este medicamento não deve ser usado por mulheres grávidas ou amamentando sem orientação médica ou do cirurgião-dentista
Interação Medicamentosa
Não existe nenhuma evidência de interações com propranolol, flunarizina, pizotifeno ou com álcool. Reações prolongadas vasoespásticas foram relatadas com a ergotamina. Como esses efeitos podem ser aditivos, deve-se esperar 24 horas antes que ao Succinato de Sumatriptana (substância ativa) possa ser utilizada após o uso de qualquer preparação contendo ergotamina.
Da mesma forma, preparações contendo ergotamina não devem ser utilizadas até seis horas após a administração do Succinato de Sumatriptana (substância ativa).
Pode ocorrer o desenvolvimento de uma interação entre o Succinato de Sumatriptana (substância ativa) e os IMAO. Assim, a administração concomitante é contraindicada.
Síndrome Serotoninérgica
Houve raros relatos pós-comercialização descrevendo pacientes com síndrome serotoninérgica (incluindo estado mental alterado, instabilidade autonômica e anormalidades neuromusculares) após o uso de ISRSs e do Succinato de Sumatriptana (substância ativa). Exemplos de IMAOs e ISRSs incluem citalopram, fluoxetina, fluvoxamina, paroxetina e sertralina.
A síndrome serotoninérgica foi também reportada após o tratamento concomitante com triptanas e IRSNs. Deve-se esperar 24 horas antes que o Succinato de Sumatriptana (substância ativa) possa ser utilizada após o uso de qualquer preparação contendo triptanas.
Ação da Substância
Resultados de eficácia
A eficácia dos comprimidos de Succinato de Sumatriptana (substância ativa) no tratamento agudo de enxaqueca foi demonstrada em 3 estudos randomizados, duplo-cegos, controlados por placebo. Os pacientes incluídos nestes 3 estudos eram predominantemente mulheres (87%) e caucasianos (97%), com uma idade média de 40 anos (intervalo de 18 a 65 anos). Os pacientes foram instruídos a tratar uma cefaleia moderada a grave. A resposta da cefaleia, definida como a redução na gravidade da cefaleia de dor moderada ou grave para dor leve ou sem dor, foi avaliada até 4 horas após a administração. Os sintomas associados, como náuseas, fotofobia e fonofobia também foram avaliados.
A manutenção da resposta foi avaliada por até 24 horas após a dose. Uma segunda dose de comprimidos de Succinato de Sumatriptana (substância ativa) ou outra medicação foi permitida 4 a 24 horas após o tratamento inicial para cefaleia recorrente.
Acetaminofeno foi oferecido aos pacientes nos Estudos 2 e 3 iniciando 2 horas após o tratamento inicial, se a dor da enxaqueca não tivesse melhorado ou tivesse piorado. Medicações adicionais foram permitidas 4 a 24 horas após o tratamento inicial para cefaleia recorrente ou como resgate em todos os 3 estudos. A frequência e tempo para uso destes tratamentos adicionais também foram determinados. Em todos os estudos, doses de 25, 50, e 100 mg foram comparadas com o placebo no tratamento de crises de enxaqueca. Em 1 estudo, doses de 25, 50, e 100 mg também foram comparadas entre si.
Em todos os 3 estudos, a porcentagem de pacientes que alcançaram resposta de cefaleia 2 e 4 horas após o tratamento foi significativamente maior entre os pacientes que receberam comprimidos de Succinato de Sumatriptana (substância ativa) em todas as doses, comparado com aqueles que receberam placebo.
Em 1 dos 3 estudos, houve uma porcentagem estatisticamente e significativamente maior de pacientes com resposta à cefaleia em 2 e 4 horas no grupo de 50 mg ou 100 mg quando comparado com os grupos de dose de 25 mg. Não foram observadas diferenças estatisticamente significativas entre os grupos de dose de 50 mg e 100 mg em nenhum dos estudos. Os resultados dos 3 estudos clínicos controlados estão resumidos na Tabela 1.
Tabela 1 – Porcentagem de pacientes com resposta de cefaleia (cefaleia leve ou sem cefaleia) 2 e 4 horas após o tratamento
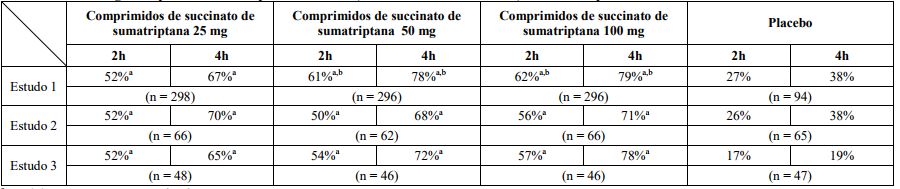
a p < 0,05 em comparação ao placebo.
b p < 0,05 em comparação a 25 mg.
A probabilidade estimada de alcançar uma resposta de cefaleia inicial ao longo de 4 horas após o tratamento nos Estudos 1, 2, e 3 agrupados é retratada na Figura 1.
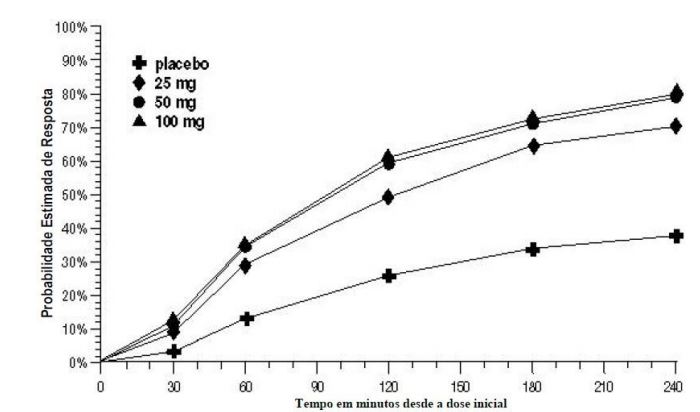
aA figura mostra a probabilidade ao longo do tempo de obter resposta de cefaleia (dor leve ou sem dor) após o tratamento com Succinato de Sumatriptana (substância ativa) oral. As médias apresentadas são baseadas nos dados agrupados dos 3 estudos clínicos controlados, fornecendo evidência de eficácia. O gráfico de Kaplan-Meier com os pacientes que não alcançaram resposta e/ou receberam resgate dentro de 240 minutos foi censurado para 240 minutos.
Para os pacientes com náuseas, fotofobia e/ou fonofobia associadas à enxaqueca no momento basal, foi observada uma menor incidência destes sintomas em 2 horas (Estudo 1) e em 4 horas (Estudos 1, 2, e 3) após a administração dos comprimidos de Succinato de Sumatriptana (substância ativa) comparado com o placebo.
Em 2 horas nos Estudos 2 e 3, ou em 4 horas no Estudo 1, durante as 24 horas após a dose inicial do tratamento do estudo, os pacientes puderam usar tratamento adicional para alívio da dor na forma de uma segunda dose do tratamento do estudo ou outra medicação. A probabilidade estimada de pacientes que receberam uma segunda dose ou outra medicação para enxaqueca ao longo de 24 horas após a dose inicial do tratamento do estudo é resumida na Figura 2.
Figura 2 – Probabilidade estimada de pacientes que receberam uma segunda dose de comprimidos de Succinato de Sumatriptana (substância ativa) ou outra medicação para tratar enxaqueca ao longo de 24 horas após a dose inicial do tratamento do estudo nos estudos 1, 2, e 3 agrupadosa
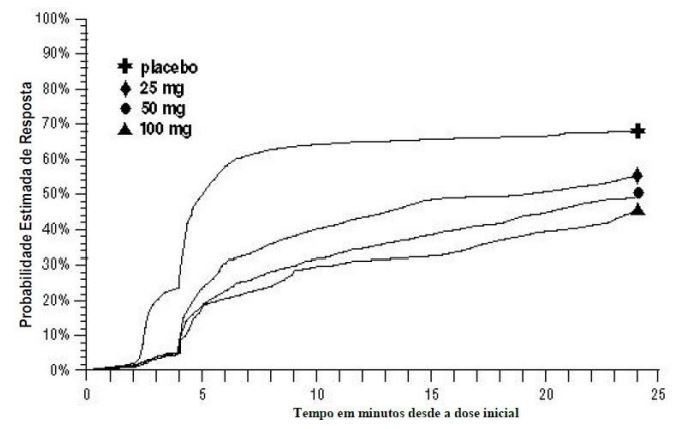
aO gráfico de Kaplan-Meier baseado nos dados obtidos nos 3 estudos clínicos controlados fornecendo evidência de eficácia com pacientes que não utilizaram tratamentos adicionais foi censurado para 24 horas. O gráfico também inclui os pacientes que não tiveram resposta à dose inicial. Não foi permitida nova medicação dentro de 2 horas após a dose.
Há evidência de que doses acima de 50 mg não oferecem um efeito superior a 50 mg. Não há evidência para sugerir que o tratamento com comprimidos de Succinato de Sumatriptana (substância ativa) estava associado com um aumento na gravidade de cefaleias recorrentes. A eficácia de comprimidos de Succinato de Sumatriptana (substância ativa) não foi afetada pela presença de aura; a duração da cefaleia antes do tratamento; gênero, idade, ou peso do indivíduo; relação com a menstruação; ou uso concomitante de medicamentos profiláticos comuns para enxaqueca (ex., betabloqueadores, bloqueadores do canal de cálcio, antidepressivos tricíclicos). Os dados foram insuficientes para avaliar o impacto da raça sobre a eficácia.
Características farmacológicas
Propriedades farmacodinâmicas
Demonstrou-se que a Succinato de Sumatriptana (substância ativa) é um agonista seletivo vascular do receptor 5-hidroxitriptamina-1- (5-HT1D), sem efeito em outros subtipos de receptores 5-HT (5- HT2-7). O receptor vascular 5 HT1D é encontrado predominantemente nos vasos sanguíneos cranianos e regulam a vasoconstrição.
Em animais, a Succinato de Sumatriptana (substância ativa) provoca constrição seletiva da circulação arterial da carótida, mas não altera o fluxo sanguíneo cerebral. A circulação arterial da carótida fornece sangue para os tecidos extracranianos e intracranianos, como as meninges. Presume-se que a dilatação e/ou a formação de edema nesses vasos esteja relacionada ao mecanismo subjacente de enxaqueca no ser humano.
Além disto, evidências experimentais sugerem que a Succinato de Sumatriptana (substância ativa) inibe a atividade do nervo trigêmeo. Essas ações podem contribuir para a ação antienxaqueca da Succinato de Sumatriptana (substância ativa) em humanos.
A resposta clínica tem início 10-15 minutos após uma injeção subcutânea com 6 mg, 15 minutos após uma dose de 20 mg fornecida por administração intranasal e aproximadamente 30 minutos após uma dose de 100 mg por via oral ou uma dose de 25 mg por via retal.
Embora a dose por via oral recomendada de Succinato de Sumatriptana (substância ativa) seja de 50 mg, as crises de enxaqueca variam em termos de gravidade num mesmo indivíduo como também entre indivíduos diferentes. As doses de 25 -100 mg mostraram uma eficácia maior do que o placebo em estudos clínicos, mas 25 mg foi menos eficaz em termos estatísticos do que 50 e 100 mg.
Propriedades farmacocinéticas
A farmacocinética da Succinato de Sumatriptana (substância ativa) não parece ser influenciada por crises de enxaqueca.
Pacientes com insuficiência hepática
Após administração oral, em pacientes com insuficiência hepática, o clearance pré-sistêmico é reduzido, resultando em aumento das concentrações plasmáticas da Succinato de Sumatriptana (substância ativa).
Cuidados de Armazenamento
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO Cuidados de armazenamento Mantenha o produto em sua embalagem original, em temperatura entre 15 e 30ºC Proteger da umidade Número de lote e datas de fabricação e validade: vide embalagem Não use medicamento com o prazo de validade vencido Guarde-o em sua embalagem original Aspectos físicos / Características Organolépticas SUTRIPTAN® 50 mg: comprimidos revestidos de cor branco SUTRIPTAN® 100 mg: comprimidos revestidos de cor rosa Antes de usar, observe o aspecto do medicamento Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo Todo medicamento deve ser mantido fora do alcance das crianças 6
Dizeres Legais
III) DIZERES LEGAIS Reg MS nº 1 0492 0170 Farm Resp : Luis Carlos de Oliveira - CRF-RJ nº 7796 Fabricado por: Cobalt Pharmaceuticals Inc 6500 Kitimat Road, Mississauga, ON L5N 2B8, Canadá Ou Fabricado por: Arrow Pharm (Malta) Ltd HF 62, Hal Far Industrial Estate, Birzebbugia BBG 3000, Malta Importado e embalado por: Actavis Farmacêutica Ltda Rua Barão de Petrópolis, 311 - Rio de Janeiro - RJ CEP 20 251-061 - CNPJ 33 150 764/0001-12 Indústria Brasileira VENDA SOB PRESCRIÇÃO MÉDICA Esta bula foi atualizada conforme Bula Padrão aprovada pela ANVISA em 12/03/14 Malta – B/MLT/SUT/VP/001 Cobalt – B2/ST/VP/001 HISTÓRICO DE ALTERAÇÃO PARA A BULA Dados da Submissão eletrônica Dados da petição/notificação que altera bula Dados das alterações de bulas Data do expediente Número do expediente Assunto Data do expediente Número do expediente Assunto Data de aprovação Itens de bula Versões (VP/VPS)
informações complementares
| Fabricante |
| BIOLAB |
| Princípio ativo |
| Succinato de sumatriptana |
| Categoria do medicamento |
| Medicamentos de A-Z |
