Preço para Janumet você encontra no CliqueFarma

R$ 276,53
RReferência
12
ofertasMelhores preços a partir de R$ 159,99 até R$ 349,00
Oferta patrocinada
vendido por Drogaria Nova Esperança
economize
20.77%
R$ 276,53
Mais de 47 anos de tradição, loja RA1000 e Ebit Diamante!
vendido por Pague Menos
economize
54.16%
R$ 159,99
vendido por Drogaria Lecer
economize
41.26%
R$ 204,99
vendido por Drogaria Primus
economize
19.01%
R$ 282,67
vendido por Sansil Farma
economize
18.21%
R$ 285,43
Frete Reduzido para o estado de São Paulo acesse e confira
vendido por Drogaria Soares
economize
12.38%
R$ 305,81
Enviamos para todo o Brasil. Clique e confira!
vendido por Farmácia Super Droga 10
economize
7.50%
R$ 322,81
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
vendido por Farmanita Drogaria
economize
2.64%
R$ 339,79
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
vendido por Pense Farma
economize
2.64%
R$ 339,79
vendido por Farmácia Indiana
economize
2.64%
R$ 339,79
vendido por Drogaria Vera Cruz
economize
2.64%
R$ 339,79
Entregas para todo o Brasil. Clique e confira!
vendido por Oncolog Medicamentos Especiais
R$ 349,00
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
Informações adicionais de Janumet - 50/1000Mg 56 Comprimidos
Qual o preço de Janumet - 50/1000Mg 56 Comprimidos?
Qual é o princípio ativo de Janumet - 50/1000Mg 56 Comprimidos?
Precisa de receita médica para comprar Janumet - 50/1000Mg 56 Comprimidos?

R$ 237,00
RReferência
10
ofertasMelhores preços a partir de R$ 229,80 até R$ 339,79
Oferta patrocinada
vendido por Drogaria São Paulo
economize
30.25%
R$ 237,00
Oferta patrocinada
vendido por Drogarias Pacheco
economize
26.43%
R$ 250,00
Oferta patrocinada
vendido por Drogaria Nova Esperança
economize
16.80%
R$ 282,70
Mais de 47 anos de tradição, loja RA1000 e Ebit Diamante!
vendido por Farmanita Drogaria
economize
32.37%
R$ 229,80
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
vendido por Drogaria Catarinense
economize
3.71%
R$ 327,19
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
vendido por Promofarma
economize
3.00%
R$ 329,60
vendido por Farmácia Preço Popular
economize
1.20%
R$ 335,70
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
vendido por Drogaria Vera Cruz
R$ 339,79
Entregas para todo o Brasil. Clique e confira!
vendido por Farmácia Indiana
R$ 339,79
vendido por NATUS FARMA
R$ 339,79
Informações adicionais de Janumet - 50/850Mg 56 Comprimidos
Veja onde comprar, qual o valor e para que serve Janumet
O que é diabetes tipo 2?
Qual a causa e fatores de risco?
- Idade acima de 45 anos
- Obesidade e sobrepeso
- Diabetes gestacional anterior
- Histórico familiar de diabetes tipo 2
- Pré-diabetes
- Sedentarismo
- Baixos níveis de colesterol HDL
- Triglicerídeos elevados
- Hipertensão
- Consumo elevado de álcool.
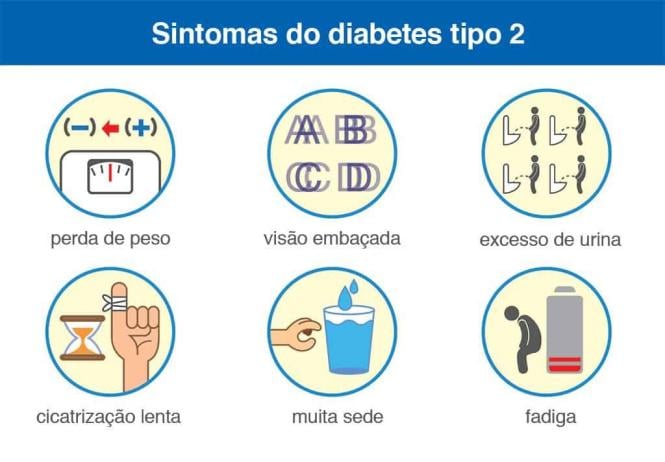
Quais os sintomas do diabetes tipo 2?
- Infecções frequentes. Alguns exemplos são bexiga, rins, pele e infecções de pele
- Feridas que demoram para cicatrizar
- Alteração visual (visão embaçada)
- Formigamento nos pés e furúnculos
- Vontade de urinar diversas vezes
- Fome frequente
- Sede constante.
Como evitar?
- Manter o peso normal
- Não fumar
- Controlar a pressão arterial
- Evitar medicamentos que potencialmente possam agredir o pâncreas
- Praticar atividade física regular.
Como Janumet funciona?
- Este medicamento também diminui os níveis de açúcar no sangue de quem tem diabetes mellitus tipo 2.
- Ele ajuda a melhorar os níveis de insulina após uma refeição.
- Janumet ajuda o organismo a responder melhor à insulina.
- Este medicamento diminui a quantidade de açúcar produzida pelo organismo.
- É incomum que Janumet cause níveis baixos de açúcar no sangue (hipoglicemia).
Posologia (Como usar) Janumet
Janumet tem efeitos colaterais?
Qual o preço de Janumet?
Onde comprar?

R$ 137,59
RReferência
2
ofertasMelhores preços a partir de R$ 137,59 até R$ 156,99
Oferta patrocinada
vendido por Drogaria São Paulo
economize
12.36%
R$ 137,59
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
Oferta patrocinada
vendido por Drogarias Pacheco
R$ 156,99
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
Informações adicionais de Sitagliptina - E Metformina Janumet 50 850 Mg Com 28 Comprimidos
Veja onde comprar, qual o valor e para que serve Janumet
O que é diabetes tipo 2?
Qual a causa e fatores de risco?
- Idade acima de 45 anos
- Obesidade e sobrepeso
- Diabetes gestacional anterior
- Histórico familiar de diabetes tipo 2
- Pré-diabetes
- Sedentarismo
- Baixos níveis de colesterol HDL
- Triglicerídeos elevados
- Hipertensão
- Consumo elevado de álcool.
Quais os sintomas do diabetes tipo 2?
- Infecções frequentes. Alguns exemplos são bexiga, rins, pele e infecções de pele
- Feridas que demoram para cicatrizar
- Alteração visual (visão embaçada)
- Formigamento nos pés e furúnculos
- Vontade de urinar diversas vezes
- Fome frequente
- Sede constante.

Como evitar?
- Manter o peso normal
- Não fumar
- Controlar a pressão arterial
- Evitar medicamentos que potencialmente possam agredir o pâncreas
- Praticar atividade física regular.
Como Janumet funciona?
- Este medicamento também diminui os níveis de açúcar no sangue de quem tem diabetes mellitus tipo 2.
- Ele ajuda a melhorar os níveis de insulina após uma refeição.
- Janumet ajuda o organismo a responder melhor à insulina.
- Este medicamento diminui a quantidade de açúcar produzida pelo organismo.
- É incomum que Janumet cause níveis baixos de açúcar no sangue (hipoglicemia).
Posologia (Como usar) Janumet
Janumet tem efeitos colaterais?
Qual o preço de Janumet?
Onde comprar?

R$ 246,50
RReferência
5
ofertasMelhores preços a partir de R$ 246,50 até R$ 336,69
Oferta patrocinada
vendido por Drogaria São Paulo
economize
26.79%
R$ 246,50
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
Oferta patrocinada
vendido por Drogarias Pacheco
economize
26.20%
R$ 248,49
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
vendido por Drogaria Lecer
economize
26.67%
R$ 246,90
vendido por Pague Menos
economize
26.05%
R$ 248,99
vendido por Farmácia Super Droga 10
R$ 336,69
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
Informações adicionais de Janumet Xr - 50/1000Mg 60 Comprimidos Liberação Prolongada
Qual o preço de Janumet Xr - 50/1000Mg 60 Comprimidos Liberação Prolongada?
Qual é o princípio ativo de Janumet Xr - 50/1000Mg 60 Comprimidos Liberação Prolongada?
Precisa de receita médica para comprar Janumet Xr - 50/1000Mg 60 Comprimidos Liberação Prolongada?

R$ 237,00
RReferência
7
ofertasMelhores preços a partir de R$ 217,50 até R$ 305,82
Oferta patrocinada
vendido por Drogaria São Paulo
economize
22.50%
R$ 237,00
Oferta patrocinada
vendido por Drogarias Pacheco
economize
18.25%
R$ 250,00
Oferta patrocinada
vendido por Drogaria Nova Esperança
economize
9.55%
R$ 276,60
Mais de 47 anos de tradição, loja RA1000 e Ebit Diamante!
vendido por Sansil Farma
economize
28.88%
R$ 217,50
Frete Reduzido para o estado de São Paulo acesse e confira
vendido por Pague Menos
economize
2.23%
R$ 298,99
vendido por Drogaria Soares
economize
0.00%
R$ 305,81
Enviamos para todo o Brasil. Clique e confira!
vendido por Farmácia Super Droga 10
R$ 305,82
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
Informações adicionais de Janumet - 50/500Mg 56Comprimidos
Qual o preço de Janumet - 50/500Mg 56Comprimidos?
Qual é o princípio ativo de Janumet - 50/500Mg 56Comprimidos?
Precisa de receita médica para comprar Janumet - 50/500Mg 56Comprimidos?

R$ 276,60
RReferência
1
ofertasMelhores preços a partir de R$ 276,60 até R$ 276,60
Oferta patrocinada
vendido por Drogaria Nova Esperança
R$ 276,60
Mais de 47 anos de tradição, loja RA1000 e Ebit Diamante!
Informações adicionais de Janumet - 50/500Mg 56 Comprimidos
Veja onde comprar, qual o valor e para que serve Janumet
O que é diabetes tipo 2?
Qual a causa e fatores de risco?
- Idade acima de 45 anos
- Obesidade e sobrepeso
- Diabetes gestacional anterior
- Histórico familiar de diabetes tipo 2
- Pré-diabetes
- Sedentarismo
- Baixos níveis de colesterol HDL
- Triglicerídeos elevados
- Hipertensão
- Consumo elevado de álcool.
Quais os sintomas do diabetes tipo 2?
- Infecções frequentes. Alguns exemplos são bexiga, rins, pele e infecções de pele
- Feridas que demoram para cicatrizar
- Alteração visual (visão embaçada)
- Formigamento nos pés e furúnculos
- Vontade de urinar diversas vezes
- Fome frequente
- Sede constante.

Como evitar?
- Manter o peso normal
- Não fumar
- Controlar a pressão arterial
- Evitar medicamentos que potencialmente possam agredir o pâncreas
- Praticar atividade física regular.
Como Janumet funciona?
- Este medicamento também diminui os níveis de açúcar no sangue de quem tem diabetes mellitus tipo 2.
- Ele ajuda a melhorar os níveis de insulina após uma refeição.
- Janumet ajuda o organismo a responder melhor à insulina.
- Este medicamento diminui a quantidade de açúcar produzida pelo organismo.
- É incomum que Janumet cause níveis baixos de açúcar no sangue (hipoglicemia).
Posologia (Como usar) Janumet
Janumet tem efeitos colaterais?
Qual o preço de Janumet?
Onde comprar?

R$ 249,42
RReferência
6
ofertasMelhores preços a partir de R$ 249,42 até R$ 326,59
Menor preço
vendido por Farmácia Indiana
economize
23.63%
R$ 249,42
vendido por Drogaria Vera Cruz
economize
19.59%
R$ 262,62
Entregas para todo o Brasil. Clique e confira!
vendido por Drogaria Catarinense
economize
14.42%
R$ 279,50
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
vendido por Farmácia Preço Popular
economize
9.19%
R$ 296,57
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
vendido por Drogaria Soares
economize
7.22%
R$ 303,02
Enviamos para todo o Brasil. Clique e confira!
vendido por Promofarma
R$ 326,59
Informações adicionais de Janumet Xr 50 1000Mg 60 Comprimidos
Veja onde comprar, qual o valor e para que serve Janumet
O que é diabetes tipo 2?
Qual a causa e fatores de risco?
- Idade acima de 45 anos
- Obesidade e sobrepeso
- Diabetes gestacional anterior
- Histórico familiar de diabetes tipo 2
- Pré-diabetes
- Sedentarismo
- Baixos níveis de colesterol HDL
- Triglicerídeos elevados
- Hipertensão
- Consumo elevado de álcool.
Quais os sintomas do diabetes tipo 2?
- Infecções frequentes. Alguns exemplos são bexiga, rins, pele e infecções de pele
- Feridas que demoram para cicatrizar
- Alteração visual (visão embaçada)
- Formigamento nos pés e furúnculos
- Vontade de urinar diversas vezes
- Fome frequente
- Sede constante.

Como evitar?
- Manter o peso normal
- Não fumar
- Controlar a pressão arterial
- Evitar medicamentos que potencialmente possam agredir o pâncreas
- Praticar atividade física regular.
Como Janumet funciona?
- Este medicamento também diminui os níveis de açúcar no sangue de quem tem diabetes mellitus tipo 2.
- Ele ajuda a melhorar os níveis de insulina após uma refeição.
- Janumet ajuda o organismo a responder melhor à insulina.
- Este medicamento diminui a quantidade de açúcar produzida pelo organismo.
- É incomum que Janumet cause níveis baixos de açúcar no sangue (hipoglicemia).
Posologia (Como usar) Janumet
Janumet tem efeitos colaterais?
Qual o preço de Janumet?
Onde comprar?

R$ 259,37
RReferência
6
ofertasMelhores preços a partir de R$ 259,37 até R$ 324,65
Oferta patrocinada
vendido por Drogaria São Paulo
economize
20.11%
R$ 259,37
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
Oferta patrocinada
vendido por Drogarias Pacheco
economize
18.58%
R$ 264,32
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
Oferta patrocinada
vendido por Drogaria Nova Esperança
economize
1.44%
R$ 319,98
Mais de 47 anos de tradição, loja RA1000 e Ebit Diamante!
vendido por Farmácia Super Droga 10
economize
13.78%
R$ 279,90
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
vendido por Drogaria Vera Cruz
economize
13.33%
R$ 281,36
Entregas para todo o Brasil. Clique e confira!
vendido por Drogaria Soares
R$ 324,65
Enviamos para todo o Brasil. Clique e confira!
Informações adicionais de Janumet Xr - 100Mg + 1000Mg Com 30 Comprimidos Revestidos De Liberação Prolongada