Comparamos o preço de Stezza 2,5 1,5Mg Com 28 Comprimidos, veja o menor preço

R$ 53,13
RReferência
2
ofertasMelhores preços a partir de R$ 47,49 até R$ 53,13
Oferta patrocinada
vendido por Drogaria Nova Esperança
R$ 53,13
Mais de 47 anos de tradição, loja RA1000 e Ebit Diamante!
vendido por Pague Menos
economize
10.62%
R$ 47,49
Para que serve
Stezza é um anticoncepcional utilizado para prevenir a gravidez.
Como o Stezza funciona?
Todos os 24 comprimidos brancos são comprimidos ativos que contêm uma pequena quantidade de dois hormônios femininos diferentes: o acetato de nomegestrol (um progestagênio) e o estradiol (o estrogênio natural).
Pílulas anticoncepcionais que contêm dois hormônios, como Stezza, são chamadas de ‘pílulas combinadas’.
O acetato de nomegestrol, o progestagênio de Stezza, é derivado do hormônio progesterona, produzido por seus ovários.
Se você utilizava pílula anteriormente, veja que Stezza contém estradiol, o estrogênio que é idêntico ao hormônio natural produzido por seus ovários, ao contrário do estrogênio sintético comumente utilizado, o etinilestradiol.
Os 4 comprimidos amarelos não contêm hormônios e são chamados de comprimidos de placebo.
Quando Stezza é tomado corretamente (sem esquecimento dos comprimidos brancos ativos), a chance de engravidar é muito pequena.
Contraindicação
Em algumas situações você não deve utilizar uma pílula combinada.
Informe seu médico se algumas das seguintes condições se aplicarem a você antes de começar a utilizar Stezza.
Ele poderá aconselhá-la a utilizar um método anticonceptivo diferente (não-hormonal).
Este medicamento é contraindicado para uso por mulheres nas seguintes condições:
- Se for alérgica ao estradiol ou ao acetato de nomegestrol, ou a qualquer um dos outros ingredientes de Stezza.
- Se tem ou teve um coágulo sanguíneo em um vaso sanguíneo (trombose venosa) das pernas, pulmões (embolia pulmonar) ou outros órgãos.
- Se teve ataque cardíaco ou derrame.
- Se tem ou teve uma condição que possa ser o primeiro sinal de ataque cardíaco (como angina do peito que causa dor torácica grave) ou derrame (como ataque isquêmico transitório ou pequeno derrame reversível).
- Se tem um distúrbio que afete a coagulação do sangue (por exemplo, deficiência de proteína C).
- Se tem ou teve um tipo de enxaqueca chamada de ‘enxaqueca com aura’.
- Se tem ou teve inflamação do pâncreas (pancreatite) associada a altas concentrações de gordura no sangue.
- Se tem ou teve doença hepática grave e seu fígado ainda não estiver funcionando normalmente.
- Se tem ou teve um tumor benigno ou maligno no fígado.
- Se tem, teve ou possa ter câncer de mama ou dos órgãos genitais.
Se tem uma doença que possa aumentar o risco de um coágulo nas artérias. Isto se aplica às seguintes doenças:
- O diabetes com vasos sanguíneos comprometidos.
- O pressão arterial muito elevada.
- O concentrações muito elevadas de gordura no sangue (colesterol ou triglicérides).
Se qualquer uma destas condições ocorrerem pela primeira vez enquanto estiver usando Stezza, interrompa o tratamento e informe seu médico.
Enquanto isso, utilize um método anticoncepcional não-hormonal.
Gravidez
Este medicamento não deve ser utilizado se você estiver grávida ou pense que possa estar grávida.
Como usar
Cuidados de administração
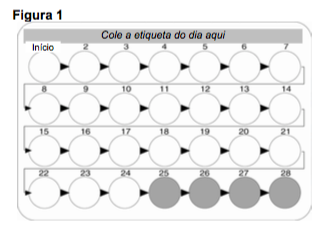
A cartela de Stezza contém 28 comprimidos: 24 comprimidos brancos com as substâncias ativas (números 1-24) e 4 comprimidos amarelos sem substâncias ativas (números 25-28).
Cada vez que iniciar uma nova cartela de Stezza, tome o comprimido branco ativo de número 1 no canto esquerdo superior. Escolha entre os 7 adesivos com indicadores de dias aquele na coluna cinza correspondente ao seu dia de início do tratamento. Por exemplo, se você começar em uma quarta-feira, utilize o adesivo que começa com ‘QUA’.
Cole-o na cartela, logo acima da fileira de comprimidos brancos ativos onde se lê ‘Cole a etiqueta aqui’. Isto possibilitará que você verifique se tomou o comprimido diário.
Tome um comprimido por dia aproximadamente no mesmo horário, com um pouco de água se necessário. Siga a direção das setas da cartela, de forma que você use os comprimidos brancos ativos primeiro e depois os comprimidos amarelos de placebo.
Sua menstruação deverá iniciar durante os 4 dias em que estiver tomando os comprimidos amarelos de placebo (chamada de sangramento de privação). Em geral, ela se inicia 2-3 dias após o último comprimido branco ativo e pode não terminar antes de você começar a nova cartela.
Comece a tomar sua próxima cartela imediatamente após o último comprimido amarelo, mesmo se sua menstruação não tenha acabado. Isto significa que você vai sempre iniciar uma nova cartela no mesmo dia da semana, e também que você irá menstruar aproximadamente nos mesmos dias de cada mês.
Algumas mulheres podem não apresentar menstruação em cada mês enquanto estiver tomando os comprimidos amarelos. Se você tomou Stezza todos os dias seguindo as instruções recomendadas, é improvável que esteje grávida.
Começando sua primeira cartela de Stezza
Se você não utilizou anticoncepcional hormonal no último mês
Comece a tomar Stezza no primeiro dia do seu ciclo (ou seja, no primeiro dia de menstruação).Stezza começa a agir imediatamente. Não é necessário usar outro método anticoncepcional.
Você também pode iniciar entre o 2° e 5° dia do seu ciclo, mas nesse caso certifique-se de usar um método anticoncepcional adicional (método de barreira) durante os primeiros 7 dias de tratamento no primeiro ciclo.
Se você utilizou outro anticoncepcional hormonal combinado (pílula anticoncepcional hormonal combinada oral (AHCO), anel vaginal ou adesivo transdérmico)
Você pode começar a tomar Stezza no dia seguinte depois de ter tomado o último comprimido da cartela que vinha utilizando (isto significa que não haverá intervalo sem tratamento). Caso a cartela que você toma contenha comprimidos inativos (placebo), você pode começar a tomar Stezza no dia seguinte depois de ter tomado o último comprimido ativo (caso você não tenha certeza sobre qual é esse comprimido, pergunte ao seu médico ou farmacêutico). Você também pode começar mais tarde, mas nunca depois do intervalo sem comprimido do seu tratamento atual (ou do dia seguinte ao do último comprimido inativo da sua pílula atual).
Caso esteja usando um anel vaginal ou um adesivo transdérmico, é melhor começar o uso de Stezza no dia da retirada do anel ou do adesivo. Você também pode iniciar, no mais tardar, no dia em que o próximo anel ou adesivo seria aplicado.
Se você usava a pílula, o adesivo ou o anel consistente e corretamente, e tiver certeza que não está grávida, você pode também parar de tomar a pílula ou retirar o anel ou adesivo em qualquer dia e iniciar o uso de Stezza imediatamente.
Se você seguir essas instruções, não será necessário utilizar um método anticoncepcional adicional.
Se você utilizou uma pílula à base de progestagênio isolado (minipílula)
Você pode parar de tomar a minipílula em qualquer dia e começar a tomar Stezza no dia seguinte, no mesmo horário. Nesse caso, certifique-se de usar um método anticoncepcional adicional (método de barreira) durante os primeiros 7 dias de tratamento com Stezza, caso tenha relações sexuais.
Se você utilizou um anticoncepcional injetável à base de progestagênio isolado, implante ou sistema intrauterino que libera progestagênio (SIU)
Comece a tomar Stezza no dia em que deveria tomar a próxima injeção ou no dia em que remover o implante ou o sistema intrauterino. Nesse caso, certifique-se de usar um método anticoncepcional adicional (método de barreira) durante os primeiros 7 dias de tratamento com Stezza, caso tenha relações sexuais.
Após o parto
Você pode começar a tomar Stezza entre os dias 21 e 28 após o parto. Se começar após o dia 28, use um método anticoncepcional adicional (método de barreira) durante os primeiros 7 dias de tratamento com Stezza. Se, após o parto, você teve relação sexual antes de começar a tomar Stezza, certifique-se que não está grávida ou espere até o próximo ciclo menstrual.
Pergunte ao seu médico o que fazer se não tiver certeza de quando começar.
Após um aborto
Seu médico vai orientá-la sobre essa questão.
Se você tiver vômitos ou diarreia intensa
Se você vomitar ou tiver diarreia intensa após tomar a pílula, os ingredientes ativos do comprimido de Stezza podem não ter sido absorvidos completamente. Se vomitar dentro de 3 a 4 horas após ter tomado o comprimido branco ativo, é como se tivesse esquecido de tomar um comprimido. Nesse caso, a confiabilidade de Stezza é mantida e você pode continuar tomando seus comprimidos seguintes no horário habitual. No entanto, se isto acontecer novamente no dia seguinte, você deverá seguir as recomendações para dois ou mais comprimidos brancos ativos esquecidos. Se tiver diarreia grave, informe seu médico.
Se você quiser atrasar a sua menstruação
Você pode atrasar a sua menstruação se continuar com os comprimidos brancos da sua próxima cartela de Stezza imediatamente após terminar os comprimidos brancos ativos da sua cartela atual.
Você pode continuar com essa cartela durante o tempo que quiser, até que ela esteja completamente vazia.
Quando quiser que sua menstruação comece, é só parar de tomar os comprimidos.
Ao usar a segunda cartela, você pode apresentar sangramento inesperado ou spotting (gotas ou manchas de sangue) durante o período em que estiver tomando os comprimidos brancos ativos.
Inicie sua próxima cartela depois do intervalo habitual de 4 dias com comprimido de placebo.
Se você quiser mudar o dia de início de sua menstruação
Se você tomar os comprimidos conforme recomendado, a menstruação ocorrerá aproximadamente no mesmo dia de cada mês.
Se quiser mudar o dia de início de sua menstruação, você poderá tornar o intervalo de comprimidos de placebo mais curto (mas nunca mais longo).
Por exemplo, se sua menstruação geralmente começa em uma sexta-feira, você pode mudar para uma terça-feira (3 dias antes) a partir do próximo mês. Simplesmente comece sua cartela seguinte 3 dias antes do que o habitual.
Se você deixar seu intervalo de comprimidos de placebo muito curto (por exemplo, 3 dias ou menos) você pode não menstruar até que tome os comprimidos amarelos de placebo ao final da segunda cartela.
No entanto, pode ocorrer sangramento inesperado ou spotting (gotas ou manchas de sangue) durante o uso dos comprimidos brancos ativos da próxima cartela.
Se você tiver um sangramento inesperado
Com todas as pílulas combinadas, nos primeiros meses de uso, pode ocorrer um sangramento vaginal irregular ou spotting (gotas ou manchas de sangue) entre as menstruações.
Poderá ser necessário o uso de absorventes, mas continue a tomar os comprimidos normalmente. Os sangramentos vaginais irregulares ou spotting normalmente param assim que o seu organismo se ajustar às pílulas (geralmente depois de cerca de 3 meses). Se o sangramento continuar, tornar-se intenso ou iniciar novamente, informe ao seu médico.
Se atrasar uma ou mais menstruações
Estudos clínicos com Stezza mostraram que você pode eventualmente não menstruar mensalmente após a tomada do comprimido branco ativo do Dia 24.
- Se você tomou todos os comprimidos corretamente, e se não vomitou ou teve diarreia intensa, nem usou outros medicamentos, então é muito improvável que esteja grávida. Continue a tomar os comprimidos de Stezza normalmente.
- Se você não tiver tomado todos os comprimidos corretamente, ou se não menstruar duas vezes seguidas, você poderá estar grávida. Informe ao seu médico imediatamente. Não inicie a próxima cartela de Stezza até que seu médico tenha verificado se você não está grávida.
Se quiser parar de tomar Stezza
Você pode parar de tomar Stezza a qualquer momento. Caso não deseje engravidar, converse com seu médico sobre outros métodos anticoncepcionais.
Se você parar de tomar Stezza porque deseja engravidar, espere até a próxima menstruação natural antes de tentar engravidar. Isso irá ajudar a calcular a data provável de nascimento do bebê.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O que devo fazer quando eu me esquecer de usar o Stezza?
Essas orientações referem-se apenas quando você se esquecer de tomar os comprimidos brancos ativos:
- Se estiver menos de 12 horas atrasada para tomar o comprimido, a confiabilidade da pílula é mantida. Tome o comprimido assim que se lembrar e tome os próximos comprimidos no horário habitual.
- Se estiver mais de 12 horas atrasada para tomar qualquer comprimido, a confiabilidade da pílula pode ficar reduzida. Quanto maior o número de comprimidos seguidos esquecidos, maior o risco de redução da eficácia anticonceptiva. Existe um risco particularmente elevado de você engravidar se esquecer de tomar os comprimidos brancos ativos do início da cartela ou do final da cartela. Portanto você deve seguir as orientações descritas a seguir.
1 comprimido branco ativo esquecido
Dias 1-24 de tomada do comprimido branco ativo (veja figura 1 e esquema)
Tome o comprimido esquecido assim que se lembrar (mesmo que isso signifique tomar dois comprimidos ao mesmo tempo) e tome os comprimidos seguintes no horário habitual.
A confiabilidade da pílula é mantida. Você não precisa tomar precauções anticoncepcionais adicionais.
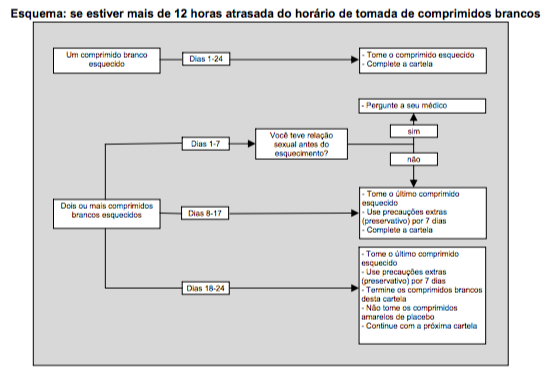
2 ou mais comprimidos brancos ativos esquecidos
Dias 1-7 de tomada do comprimido branco ativo (veja figura 1 e esquema)
Tome o último comprimido branco ativo esquecido assim que se lembrar (mesmo que isso signifique tomar dois comprimidos ao mesmo tempo) e tome os comprimidos seguintes no horário habitual.
No entanto, utilize precauções anticoncepcionais adicionais (método de barreira) pelos 7 dias seguintes. Se você teve relação sexual na semana anterior ao esquecimento dos comprimidos, existe a possibilidade de você engravidar ou estar grávida. Entre em contato com seu médico imediatamente.
Dias 8-17 de tomada do comprimido branco ativo (veja figura 1 e esquema)
Tome o último comprimido branco ativo esquecido assim que se lembrar (mesmo que isso signifique tomar dois comprimidos ao mesmo tempo) e tome os comprimidos seguintes no horário habitual. Utilize precauções anticoncepcionais adicionais (método de barreira) pelos 7 dias seguintes.
Dias 18-24 de tomada do comprimido branco ativo (veja figura 1 e esquema)
Existe um risco particularmente elevado de você engravidar se esquecer de tomar os comprimidos brancos ativos próximo ao intervalo de comprimidos amarelos de placebo. Ao ajustar o esquema de tomada dos comprimidos, este risco mais elevado pode ser prevenido.
Tome o último comprimido branco ativo esquecido assim que se lembrar (mesmo que isso signifique tomar dois comprimidos ao mesmo tempo) e tome os comprimidos seguintes no horário habitual. Utilize precauções anticoncepcionais adicionais (método de barreira) pelos 7 dias seguintes.
Comece a cartela seguinte assim que os comprimidos brancos ativos da cartela atual tiverem acabado, portanto, nenhum comprimido amarelo de placebo deve ser tomado. Você poderá não menstruar até que tome os comprimidos amarelos de placebo do final da segunda cartela, mas poderá apresentar spotting (gotas ou manchas de sangue) ou sangramento inesperado enquanto estiver tomando os comprimidos brancos ativos.
Se não conseguir lembrar quantos comprimidos brancos ativos foram esquecidos, utilize precauções anticoncepcionais adicionais (método de barreira) pelos 7 dias seguintes e entre em contato com seu médico imediatamente.
Se tiver esquecido de tomar os comprimidos brancos ativos de uma cartela e não apresentar a menstruação mensal esperada durante a tomada dos comprimidos amarelos de placebo da mesma cartela, pode ser que esteja grávida. Consulte seu médico antes de começar a tomar a próxima cartela.
1 ou mais comprimidos amarelos de placebo esquecidos
Os últimos 4 comprimidos amarelos da quarta fileira são comprimidos de placebo que não contêm substâncias ativas. Se você esqueceu de tomar um destes comprimidos, a confiabilidade de Stezza é mantida.
Jogue fora o(s) comprimido(s) amarelo(s) de placebo que você se esqueceu de tomar e continue a tomar os comprimidos seguintes no horário habitual.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
Precauções
Notas gerais
Antes que você inicie o tratamento com Stezza, seu médico fará algumas perguntas sobre seu histórico de saúde e o de seus parentes próximos. O médico também medirá sua pressão arterial e, dependendo de sua situação pessoal, também poderá realizar outros exames.
Nesta bula são descritas várias situações nas quais você deve interromper o uso da pílula ou nas quais a confiabilidade da pílula possa estar reduzida. Nessas situações, você não deve ter relações sexuais ou deve adotar precauções anticonceptivas adicionais não-hormonais, como por exemplo, o uso de preservativo ou outro método de barreira.
Não use o método de medição de temperatura ou rítmico. Estes métodos podem não ser confiáveis porque a pílula altera as oscilações normais de temperatura e do muco cervical que ocorrem durante o ciclo menstrual.
Stezza, assim como outros anticoncepcionais hormonais, não protege contra infecção por HIV (AIDS) ou qualquer outra doença sexualmente transmissível.
Tome cuidado especial com Stezza
Em algumas situações, você precisa ter cuidado especial enquanto estiver usando uma pílula combinada.
Informe seu médico se alguma das seguintes condições se aplicarem a você. Caso alguma delas se desenvolva ou piore durante o uso de Stezza, você deverá informar seu médico.
- Se tiver angioedema hereditário. Consulte seu médico imediatamente se apresentar sintomas de angioedema, como inchaço da face, língua e/ou garganta e/ou dificuldade para engolir ou urticária, acompanhado de dificuldade para respirar. Produtos contendo estrogênios podem induzir ou piorar esses sintomas;
- Se um parente próximo tem ou já teve câncer de mama;
- Se tem epilepsia;
- Se tem doença hepática (por exemplo, icterícia) ou doença da vesícula biliar (por exemplo, cálculos biliares);
- Se tem diabetes;
- Se tem depressão;
- Se tem doença de Crohn ou colite ulcerativa (doença intestinal inflamatória crônica);
- Se tem lúpus eritematoso sistêmico, uma doença que afeta seu sistema de defesa natural;
- Se tem síndrome urêmica hemolítica, um distúrbio de coagulação sanguínea que causa insuficiência dos rins;
- Se tem anemia falciforme (uma doença hereditária das hemácias);
- Se tem concentrações elevadas de ácidos graxos no sangue (hipertriglideridemia) ou um histórico familiar positivo para esta condição (hipertrigliceridemia familiar). Se esse for o caso, você pode ter um risco aumentado de desenvolver pancreatite (inflamação do pâncreas) ao usar pílulas combinadas;
- Se tem uma condição que ocorreu pela primeira vez ou piorou durante a gravidez ou uso prévio de hormônios sexuais (p.ex., perda da audição, porfiria (uma doença sanguínea), herpes gestacional (erupção cutânea com vesículas durante a gravidez), coreia de Sydenham (uma doença dos nervos na qual ocorrem movimentos corporais repentinos);
- Se tem ou teve cloasma (manchas de pigmentos marrom-amarelados, chamadas de ‘manchas de gravidez’, particularmente na face). Se esse for o caso, evite exposição excessiva ao sol ou à luz ultravioleta;
- Se precisar passar por uma cirurgia ou imobilização prolongada.
Coágulos sanguíneos (trombose)
Coágulos sanguíneos em uma veia
Um coágulo sanguíneo em uma veia (conhecido como trombose venosa) pode bloquear a veia. Isto pode ocorrer nas veias das pernas, pulmões (embolia pulmonar) ou qualquer outro órgão.
O uso de pílula combinada contendo etinilestradiol aumenta o risco da usuária desenvolver coágulos em comparação com não-usuárias. O risco de desenvolver um coágulo sanguíneo em uma veia é mais elevado durante o primeiro ano em que uma mulher usa a pílula. O risco não é tão elevado quanto o risco de desenvolver um coágulo sanguíneo durante a gravidez.
Stezza contém estradiol em vez do etinilestradiol. Ainda não se sabe como Stezza influencia o risco de desenvolver coágulo sanguíneo em comparação com outras pílulas anticoncepcionais.
O risco de coágulos sanguíneos em uma veia aumenta:
- Com o aumento da idade;
- Se um de seus parentes próximos teve coágulo sanguíneo nas pernas, pulmões ou outros órgãos em uma idade relativamente precoce;
- Se for obesa;
- Se tiver que ser submetida a uma cirurgia ou imobilização por longo período devido a uma lesão ou doença, ou se tiver sua perna engessada.
Se isto se aplicar a você, é importante informar seu médico que está usando Stezza, uma vez que o tratamento poderá ser interrompido.
Seu médico irá orientá-la sobre a interrupção do tratamento anticoncepcional hormonal várias semanas antes da cirurgia ou enquanto estiver mobilizada.
Seu médico informará também quando você pode reiniciar o tratamento com Stezza, assim que estiver se movimentando normalmente.
Coágulos sanguíneos em uma artéria
Um coágulo sanguíneo em uma artéria pode causar sérios problemas. Por exemplo, um coágulo sanguíneo em uma artéria no coração causa ataque cardíaco e no cérebro, causa um derrame.
O risco de um coágulo sanguíneo em uma artéria aumenta:
- Com o aumento da idade;
- Se for fumante. Ao utilizar um anticoncepcional hormonal como Stezza você é fortemente aconselhada a parar de fumar, especialmente se tiver mais de 35 anos de idade;
- Se tiver sobrepeso;
- Se tiver pressão alta;
- Se um parente próximo tiver sofrido um ataque cardíaco ou um derrame em idade precoce;
- Se tiver concentrações elevadas de gordura no sangue (colesterol ou triglicérides);
- Se tiver enxaquecas;
- Se tiver um problema cardíaco (distúrbio valvular ou do ritmo).
Sintomas de coágulos sanguíneos
Pare de tomar comprimidos e consulte seu médico imediatamente se perceber possíveis sinais de um coágulo sanguíneo, como:
- Tosse súbita incomum;
- Dor intensa no tórax que pode atingir o braço esquerdo;
- Falta de ar;
- Qualquer dor de cabeça incomum, intensa ou duradoura, ou piora da enxaqueca;
- Perda de visão parcial ou completa, ou visão dupla;
- Fala pouco clara ou incapacidade para falar;
- Alterações repentinas de audição, olfato ou paladar;
- Tontura ou desmaio;
- Fraqueza ou dormência em qualquer parte do corpo;
- Dor intensa no abdômen;
- Dor ou inchaço intenso em qualquer uma de suas pernas.
Após um coágulo sanguíneo, a recuperação nem sempre é completa. Raramente podem ocorrer incapacidades permanentes graves ou o coágulo sanguíneo pode até ser fatal.
Logo após o parto, as mulheres apresentam risco elevado de coágulos sanguíneos, assim, você deve perguntar ao seu médico quando pode começar a tomar uma pílula combinada após o parto.
Câncer
As informações fornecidas a seguir foram obtidas de estudos com pílulas combinadas contendo etinilestradiol, mas também podem se aplicar a Stezza.
O câncer de mama foi diagnosticado um pouco mais frequentemente em mulheres que utilizam pílulas combinadas, mas não se sabe se isso é causado pelo tratamento.
Por exemplo, pode ser que os tumores sejam diagnosticados em maior frequência em mulheres que tomam pílulas combinadas porque elas são examinadas frequentemente pelo médico. O aumento da ocorrência de câncer de mama torna-se gradualmente menor depois da interrupção do tratamento com a pílula combinada.
É importante verificar regularmente os seus seios e contatar seu médico caso note qualquer nódulo. Informe seu médico se um parente próximo tem ou teve câncer de mama.
Em casos raros de usuárias de pílulas foram relatados tumores hepáticos benignos (não cancerosos) e, ainda mais raramente, tumores hepáticos malignos (cancerosos). Contate seu médico se apresentar dor abdominal incomum e intensa.
O câncer cervical é causado por uma infecção pelo papilomavírus humano (HPV). Foi relatado que ocorre mais frequentemente em mulheres que usam a pílula por longo período.
Não se sabe se este achado é devido ao uso de anticoncepcionais hormonais ou ao comportamento sexual e a outros fatores (tais como uma melhor triagem cervical).
Para usuárias de pílulas combinadas de alta dose de etinilestradiol foi relatado que câncer endometrial (revestimento do útero) e câncer de ovário ocorrem com menor frequência.
Isso também pode ser o caso para pílulas contendo baixas doses de etinilestradiol e pílulas contendo o estradiol natural, mas isso não foi confirmado.
Exames laboratoriais
Se precisar fazer exame de sangue ou urina, informe ao seu médico que está utilizando Stezza, uma vez que o produto pode alterar os resultados de alguns exames.
Informações à paciente
Recomenda-se a leitura cuidadosa desta bula antes de iniciar o tratamento com este medicamento.
- Guarde esta bula. Você poderá precisar ler as informações novamente em outra ocasião.
- Se você tiver alguma dúvida, peça auxílio ao seu médico ou farmacêutico.
- Este medicamento foi receitado para você e não deve ser fornecido a outras pessoas, pois pode ser prejudicial a elas.
- Se algum dos efeitos colaterais tornar-se grave ou se você apresentar algum efeito colateral que não seja mencionado nesta bula, informe ao seu médico ou farmacêutico.
Informações importantes sobre alguns dos ingredientes de Stezza
Stezza contém lactose. Se você tem intolerância a alguns açúcares, entre em contato com o seu médico antes de começar o tratamento com Stezza.
Quando você deve contatar o seu médico?
Exames regulares
Enquanto você estiver usando a pílula, seu médico solicitará seu retorno para realizar exames regulares. Em geral, você deve realizar uma bateria de exames anualmente.
Contate o seu médico assim que possível:
- Se perceber qualquer alteração na sua saúde, especialmente envolvendo qualquer um dos itens mencionados nesta bula;
- Se sentir nódulos em seu seio;
- Se apresentar sintomas de angioedema como inchaço da face, língua e/ou garganta e/ou dificuldade para engolir ou urticária juntamente com dificuldade para respirar;
- Se for utilizar outros medicamentos;
- Se sua capacidade de se movimentar estiver limitada por um longo período de tempo ou se você for submetida a uma cirurgia (informe ao seu médico com pelo menos quatro semanas de antecedência);
- Se apresentar sangramento vaginal intenso incomum;
- Se esquecer de tomar um ou mais comprimidos da cartela na primeira semana e tiver tido relações sexuais sem proteção nos sete dias anteriores;
- Se tiver diarreia intensa;
- Se a sua menstruação atrasar e houver suspeita de gravidez.
Pare de tomar os comprimidos e contate o seu médico imediatamente se perceber possíveis sinais de um coágulo sanguíneo.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento. Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Reações Adversas
Assim como todos os medicamentos, Stezza pode causar eventos adversos embora nem todas as pessoas os apresentem.
Contate seu médico se perceber algum efeito indesejável, especialmente se forem graves ou persistentes, ou se houver alguma alteração na sua saúde que você julgue que possa ser causada pela pílula.
As seguintes reações adversas foram associadas ao uso de Stezza:
Muito comum (afeta mais de 1 mulher em 10)
- Acne;
- Alterações de ciclo menstrual (p.ex., ausência de menstruação ou sangramento de privação/spotting (gotas ou manchas de sangue)).
Comum (afeta 1 a 10 mulheres em 100)
- Diminuição/perda de interesse por sexo;
- Depressão/humor deprimido, alterações de humor;
- Dor de cabeça ou enxaqueca (incluindo enxaqueca com aura);
- Sensação de enjoo (náusea);
- Menstruações intensas;
- Dor/desconforto/sensibilidade nas mamas;
- Dor pélvica, desconforto pélvico;
- Ganho de peso.
Incomum (afeta 1 a 10 mulheres em 1.000)
- Aumento do apetite, desejo por alimentos;
- Retenção hídrica (edema);
- Fogacho (ondas de calor);
- Abdome inchado, excesso de gás no estômago ou no intestino;
- Aumento de transpiração, sudorese noturna, perda de cabelo, coceira, pele seca, pele oleosa;
- Sensação de peso nos membros;
- Menstruações regulares mas escassas; menstruação irregular;
- Aumento da mama;
- Nódulo na mama; produção de leite embora não esteja grávida;
- Síndrome pré-menstrual;
- Dor durante a relação sexual; secura na vagina ou vulva;
- Espasmo do útero;
- Irritabilidade;
- Aumento de enzimas hepáticas.
Raro (afeta 1 a 10 mulheres em 10.000)
- Diminuição do apetite;
- Aumento do interesse por sexo;
- Distúrbio de atenção;
- Olho seco, intolerância a lentes de contato;
- Boca seca;
- Manchas de pigmento marrom-douradas, principalmente na face;
- Excessivo crescimento de cabelo;
- Odor vaginal, desconforto/dor na vagina ou vulva;
- Fome.
Reações alérgicas (hipersensibilidade) tem sido relatadas em usuárias de Stezza, porém a frequência não consegue ser estimada a partir dos dados disponíveis.
Se alguma das reações adversas ficarem graves, ou se você perceber alguma reação adversa que não esteja listada nesta bula, informe seu médico ou farmacêutico.
Atenção: este produto é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe seu médico ou cirurgião-dentista.
População Especial
Uso em adolescentes
Nenhum dado de eficácia e segurança está disponível em adolescentes com menos de 18 anos de idade.
Gravidez
Stezza não deve ser utilizado por mulheres grávidas ou que pensem que possam estar grávidas. Caso você engravide enquanto estiver utilizando Stezza, interrompa o tratamento e contate seu médico.
Este medicamento causa malformação ao bebê durante a gravidez.
Lactação
Stezzanão é recomendado para uso durante a amamentação. Caso deseje utilizar a pílula enquanto estiver amamentando, procure aconselhamento com seu médico.
Dirigir e operar máquinas
Stezza é improvável de afetar sua capacidade de dirigir ou operar máquinas.
Composição
Stezza 2,5 mg + 1,5 mg
Cada comprimido revestido branco contém:
| Acetato de nomegestrol | 2,5 mg |
| Estradiol hemi-hidratado | 1,5 mg |
Excipientes: lactose monoidratada, celulose microcristalina, crospovidona, talco, estearato de magnésio, sílica coloidal anidra, álcool polivinílico, dióxido de titânio e macrogol.
Cada comprimido revestido amarelo contém:
Excipientes: lactose monoidratada, celulose microcristalina, crospovidona, talco, estearato de magnésio, sílica coloidal anidra, álcool polivinílico, dióxido de titânio, macrogol, óxido de ferro amarelo e óxido de ferro preto.
Superdosagem
Não houve relato de efeitos prejudiciais sérios com a ingestão de muitos comprimidos de Stezza de uma só vez.
Se você tiver tomado vários comprimidos de uma só vez, poderá apresentar náusea, vômitos ou sangramento vaginal.
Se você descobrir que uma criança tomou Stezza, peça aconselhamento médico.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
Interação Medicamentosa
Influência de outros medicamentos sobre Acetato de Nomegestrol + Estradiol (substâncias ativas)
Interações entre anticoncepcionais orais e medicamentos indutores enzimáticos podem causar sangramento inesperado e falha anticonceptiva.
Exemplos de substâncias ativas que induzem enzimas hepáticas e, assim, resultam em aumento da depuração dos hormônios sexuais são: fenitoína, fenobarbital, primidona, bosentana, carbamazepina, rifampicina e medicamentos ou preparações à base de plantas contendo ervade-são-joão, e, em menor extensão, oxcarbazepina, topiramato, felbamato e griseofulvina. Adicionalmente, inibidores da protease HIV com um potencial indutor (por exemplo, ritonavir e nelfinavir) e inibidores não nucleosídicos da transcriptase reversa (por exemplo, nevirapina e efavirenz) podem afetar o metabolismo hepático.
Com substâncias indutoras de enzimas hepáticas, um método de barreira deve ser utilizado durante o tempo de administração concomitante do medicamento e nos 28 dias após a sua descontinuação. Em caso de tratamento prolongado com substâncias indutoras de enzimas hepáticas, outro método anticoncepcional deve ser considerado.
Estudos de interação medicamentosa não foram realizados com Acetato de Nomegestrol + Estradiol (substâncias ativas), mas dois estudos com rifampicina e cetoconazol, respectivamente, foram realizados com doses mais elevadas de combinação de Acetato de Nomegestrol/estradiol (Acetato de Nomegestrol 3,75 mg + 1,5 mg de estradiol) em mulheres na pós-menopausa.
O uso concomitante de rifampicina diminui a AUC0-? de Acetato de Nomegestrol em 95% e aumenta a AUC0-túltimo de estradiol em 25%.
O uso concomitante de cetoconazol (dose única de 200 mg) não modifica o metabolismo do estradiol, mas foram observados aumentos no pico de concentração (85%) e de AUC0-? (115%) de Acetato de Nomegestrol, os quais não tiveram relevância clínica. Conclusões similares são esperadas em mulheres em idade fértil.
Influência de Acetato de Nomegestrol + Estradiol (substâncias ativas) sobre outros medicamentos
Os anticoncepcionais orais podem afetar o metabolismo de outros medicamentos.
Deve-se dar atenção especial para a interação com a lamotrigina.
Outras interações
Durante estudos clínicos com combinações de medicamentos utilizados no tratamento do vírus de hepatite C (HCV) ombitasvir/paritaprevir/ritonavir com ou sem dasabuvir, aumentos de ALT maior que 5 vezes o limite superior da normalidade (LSN) foi significativamente mais frequente em mulheres utilizando medicamentos contendo etinilestradiol, tais como os ACHs.
Mulheres utilizando medicamentos contendo estrogênios excetuando o etinilestradiol, tal como o estradiol, tiveram uma taxa de aumento de ALT similar àquelas que não receberam estrogênio; porém, devido ao número limitado de mulheres usando esses outros estrogênios, recomenda-se precaução na coadministração com combinações de regime de tratamento com medicamentos contendo ombitasvir/paritaprevir/ritonavir com ou sem dasabuvir.
Exames laboratoriais
O uso de AHCOs pode influenciar os resultados de certos exames laboratoriais, incluindo parâmetros bioquímicos hepáticos, da tireoide, adrenais e renais, concentrações plasmáticas de proteínas (carreadoras), por exemplo, globulinas transportadoras de corticosteroide e de frações de lipídeos/lipoproteínas, parâmetros de metabolismo de carboidratos, e parâmetros de coagulação e fibrinólise. As alterações geralmente permanecem dentro da faixa laboratorial normal.
Ação da Substância
Resultados de Eficácia
Em dois estudos randomizados, abertos e comparativos de eficácia-segurança, mais de 3.200 mulheres entre 18-50 anos de idade foram tratadas por até 13 ciclos consecutivos com Acetato de Nomegestrol + Estradiol (substâncias ativas) e mais de 1.000 mulheres com drospirenona 3 mg-etinilestradiol 30 mcg (regime de 21/7).
No grupo de Acetato de Nomegestrol + Estradiol (substâncias ativas), foi relatado aumento de peso em 8,6% das mulheres (versus 5,7% no grupo comparador); sangramento de privação anormal (predominantemente ausência de sangramento de privação) em 10,5% das mulheres (versus 0,5% no grupo comparador); e acne em 15,4% das mulheres (versus 7,9% no grupo comparador). As avaliações de acne durante o tratamento com Acetato de Nomegestrol + Estradiol (substâncias ativas) mostraram que a maioria das mulheres (73,1%) não apresentou alteração no status da acne em comparação com o pré- tratamento, enquanto 16,8% apresentaram melhora da acne e 10,1% apresentaram novos casos ou agravamento da acne.
Para o comparador drospirenona 3 mg – etinilestradiol 30 mcg, cuja menor dose tem a indicação para o tratamento da acne, 75,4% das mulheres não apresentaram alteração no status da acne, enquanto 20,4% apresentaram melhora e 4,2% apresentaram agravamento da acne.
No estudo clínico realizado com Acetato de Nomegestrol + Estradiol (substâncias ativas) na União Europeia, Ásia e Austrália, foram calculados os seguintes índices de Pearl para a faixa etária de 18-35 anos:
- Falha do método: 0,40 (limite superior do intervalo de confiança 95%: 1,03);
- Falha do método e da usuária: 0,38 (limite superior do intervalo de confiança 95%: 0,97).
No estudo clínico realizado com Acetato de Nomegestrol + Estradiol (substâncias ativas) nos Estados Unidos, Canadá e América Latina, foram calculados os seguintes índices de Pearl para a faixa etária de 18-35 anos:
- Falha do método: 1,22 (limite superior do intervalo de confiança 95%: 2,18);
- Falha do método e da usuária: 1,16 (limite superior do intervalo de confiança 95%: 2,08).
Em um estudo randomizado e aberto, 32 mulheres foram tratadas por 6 ciclos com Acetato de Nomegestrol + Estradiol (substâncias ativas).
Após a descontinuação de Acetato de Nomegestrol + Estradiol (substâncias ativas), o retorno da ovulação ocorreu em média 20,8 dias após a última tomada de comprimido, sendo que as ovulações mais precoces foram detectadas em 16 dias.
O ácido fólico é uma vitamina importante na fase inicial da gravidez. As concentrações séricas de ácido fólico permaneceram inalteradas durante e após o tratamento com Acetato de Nomegestrol + Estradiol (substâncias ativas) por 6 ciclos consecutivos em comparação com o basal.
Em um estudo randomizado, aberto e comparativo de 2 anos, mulheres de 21-35 anos de idade foram tratadas com Acetato de Nomegestrol + Estradiol (substâncias ativas) sem efeito clinicamente relevante sobre a densidade mineral óssea.
Um estudo randomizado, aberto, comparativo e multicêntrico foi realizado para determinar os efeitos de Acetato de Nomegestrol + Estradiol (substâncias ativas) sobre hemostasia, lipídios, metabolismo de carboidratos, função adrenal e da tireoide, e androgênios. Sessenta mulheres de 18-50 anos de idade foram tratadas com Acetato de Nomegestrol + Estradiol (substâncias ativas) por 6 ciclos consecutivos.
Tolerância à glicose e sensibilidade à insulina permaneceram inalteradas e nenhum efeito clinicamente relevante sobre o metabolismo lipídico e a hemostasia foi observado. Acetato de Nomegestrol + Estradiol (substâncias ativas) aumentou as proteínas carreadoras TBG e CBG, e induziu um pequeno aumento de SHBG. Os parâmetros androgênicos androstenediona, DHEA-S, testosterona total e livre foram significativamente reduzidos durante o uso de Acetato de Nomegestrol + Estradiol (substâncias ativas).
A histologia endometrial foi investigada em um subgrupo de mulheres (n = 32) em um estudo clínico após 13 ciclos de tratamento. Não houve qualquer resultado anormal.
População pediátrica
Não há dados disponíveis sobre eficácia e segurança em adolescentes com menos de 18 anos de idade. Os dados farmacocinéticos disponíveis estão descritos no item "Características farmacológicas - Farmacocinética".
Características farmacológicas
Farmacocinética
Acetato de Nomegestrol (NOMAC)
Absorção
O Acetato de Nomegestrol administrado por via oral é rapidamente absorvido. Concentrações plasmáticas máximas de aproximadamente 7 ng/mL são atingidas em 2 h após administração única.
A biodisponibilidade absoluta após uma dose única é de 63%. Nenhum efeito clinicamente relevante dos alimentos foi observado sobre a biodisponibilidade do Acetato de Nomegestrol .
Distribuição
O Acetato de Nomegestrol se liga extensivamente à albumina (97-98%), mas não se liga à globulina ligadora de hormônios sexuais (SHBG) ou à globulina ligadora de corticoide (CBG). O volume de distribuição aparente do Acetato de Nomegestrol no estado de equilíbrio é de 1.645 ± 576 L.
Biotransformação
O cetato de Nomegestrol é metabolizado em diversos metabólitos hidroxilados inativos pelas enzimas hepáticas do citocromo P450, principalmente a CYP3A4 e a CYP3A5 com possível contribuição da CYP2C19 e da CYP2C8. O Acetato de Nomegestrol e seus metabólitos hidroxilados sofrem amplo metabolismo de fase 2 para formar conjugados glicurônicos e de sulfato. A depuração aparente no estado de equilíbrio é de 26 L/h.
Eliminação
A meia-vida de eliminação (t1/2) é de 46 h (variando de 28-83 h) no estado de equilíbrio. A meia-vida de eliminação dos metabólitos não foi determinada.
O Acetato de Nomegestrol é excretado pela urina e pelas fezes. Aproximadamente 80% da dose é excretada na urina e nas fezes dentro de 4 dias. A excreção do Acetato de Nomegestrol foi quase completa após 10 dias e as quantidades excretadas foram maiores nas fezes do que na urina.
Linearidade
Observou-se linearidade de dose na faixa de 0,625-5 mg (determinada em mulheres férteis e pós-menopáusicas).
Condições no estado de equilíbrio
A farmacocinética do Acetato de Nomegestrol não é influenciada pela SHBG. O estado de equilíbrio é atingido após 5 dias. Concentrações plasmáticas máximas de aproximadamente 12 ng/mL são atingidas 1,5 h após a administração. As concentrações médias plasmáticas de estado de equilíbrio são de 4 ng/mL.
Interações medicamentosas
O Acetato de Nomegestrol não causa indução ou inibição observável in vitro de qualquer enzima do citocromo P450 e não apresenta interação clinicamente relevante com o transportador P-gp.
Estradiol (E2)
Absorção
Após administração oral, o Estradiol sofre considerável efeito de primeira passagem. A biodisponibilidade absoluta é de aproximadamente 1%. Nenhum efeito clinicamente relevante da presença de alimentos foi observado sobre a biodisponibilidade do Estradiol.
Distribuição
A distribuição de Estradiol exógeno e endógeno é similar. Os estrogênios são amplamente distribuídos no organismo e são, em geral, encontrados em maiores concentrações nos órgãos-alvo de hormônios sexuais. O Estradiol circula no sangue ligado à SHBG (37%) e à albumina (61%), enquanto apenas aproximadamente 1-2% fica livre.
Biotransformação
O Estradiol exógeno oral é amplamente metabolizado. O metabolismo do Estradiol exógeno e endógeno é similar. O Estradiol é rapidamente transformado no intestino e no fígado em vários metabólitos, principalmente em estrona, os quais são subsequentemente conjugados e passam por circulação entero-hepática. Existe um equilíbrio dinâmico entre o Estradiol, a estrona e a estrona-sulfato devido a várias atividades enzimáticas incluindo Estradiol-desidrogenases, sulfotransferases e arilsulfatases.
A oxidação da estrona e do Estradiol envolve as enzimas do citocromo P450, principalmente CYP1A2, CYP1A2 (extra-hepática), CYP3A4, CYP3A5, CYP1B1 e CYP2C9.
Eliminação
O Estradiol é rapidamente depurado da circulação. Devido ao metabolismo e à circulação entero-hepática, um grande grupo circulante de sulfatos e glicuronídeos estrogênicos está presente. Isso resulta em uma meia-vida de eliminação corrigida pelo nível basal altamente variável de estradiol, que é calculada como sendo de 3,6 ± 1,5 h após administração intravenosa.
Condições no estado de equilíbrio
As concentrações séricas máximas de Estradiol são de aproximadamente 90 pg/mL e são atingidas 6 h após a administração. As concentrações séricas médias são de 50 pg/mL e essas concentrações de Estradiol correspondem às das fases inicial e tardia do ciclo menstrual de uma mulher.
Populações especiais
População pediátrica
A farmacocinética do Acetato de Nomegestrol (objetivo primário) após uma única administração oral de Acetato de Nomegestrol + Estradiol (substâncias ativas) em mulheres saudáveis adultas e adolescentes pós-menarca foi similar. A exposição ao Estradiol (objetivo secundário) foi similar em mulheres adolescentes versus adultas durante as primeiras 24 horas, e menor após 24 horas. A relevância clínica desse resultado é desconhecida.
Efeito da insuficiência renal
Não foi realizado estudo para avaliar o efeito da doença renal sobre a farmacocinética de Acetato de Nomegestrol + Estradiol (substâncias ativas).
Efeito da insuficiência hepática
Não foi conduzido estudo para avaliar o efeito da doença hepática sobre a farmacocinética de Acetato de Nomegestrol + Estradiol (substâncias ativas). No entanto, os hormônios esteroides podem ser pouco metabolizados em mulheres com insuficiência hepática.
Grupos étnicos
Não foi realizado estudo formal para determinar a farmacocinética em grupos étnicos.
Cuidados de Armazenamento
Conservar em temperatura ambiente (entre 15 e 30°C).
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Aspecto dos comprimidos revestidos de Stezza:
Ativos
Os comprimidos ativos são brancos, redondos com 5,5 mm de diâmetro. Os comprimidos são codificados com ‘ne’ em ambos os lados.
Placebo
Os comprimidos de placebo são amarelos, redondos com 5,5 mm de diâmetro. Os comprimidos são codificados com ‘p’ em ambos os lados.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
Dizeres Legais
Venda sob prescrição médica.
MS 1.0029.0186
Farmacêutico Responsável:
Fernando C. Lemos
CRF-SP n° 16.243
Registrado e importado por:
Merck Sharp & Dohme Farmacêutica Ltda.
Rua 13 de Maio, 815 - Sousas, Campinas/SP
CNPJ: 45.987.013/0001-34
Brasil
MSD On line 0800-0122232
e-mail: [email protected]
www.msdonline.com.br
Fabricado e embalado por:
Organon Ireland Ltd.
Drynam Road, Swords, Co. Dublin - Irlanda